
题目列表(包括答案和解析)
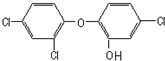 三氯生是一种抗菌剂,结构如图所示.美国弗吉尼亚理工大学教师比德的一项实验表明,含有三氯生的产品与含氯的自来水发生反应后,可形成三氯甲烷(氯仿).氯仿曾被用作麻醉剂,动物试验发现,氯仿会对心脏和肝脏造成损伤,具有轻度致畸性,可诱导小白鼠发生肝癌.下列说法正确的是( )
三氯生是一种抗菌剂,结构如图所示.美国弗吉尼亚理工大学教师比德的一项实验表明,含有三氯生的产品与含氯的自来水发生反应后,可形成三氯甲烷(氯仿).氯仿曾被用作麻醉剂,动物试验发现,氯仿会对心脏和肝脏造成损伤,具有轻度致畸性,可诱导小白鼠发生肝癌.下列说法正确的是( )| A、三氯生的分子式是C12H6Cl3O2 | B、三氯生不与浓溴水发生反应 | C、氯仿与甲烷均为正四面体结构 | D、1mol三氯生最多可与7mol NaOH反应 |


| O | 3 |
| O | 3 |
| O | 2 |
(15分)无水硫酸铜在加热条件下能发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气。某学生试图用下图所示装置来确定该化学反应中各物质的计量关系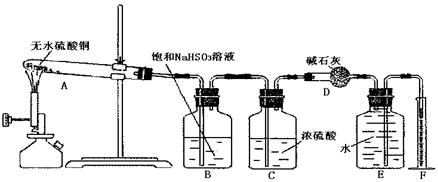
试回答:
(1)加热过程中,试管A中发生的实验现象为 。
(2)装置E和F的作用是 ;
(3)该学生使用装置B的本意是除去混合气体中的三氧化硫以提纯氧气,他的做法正确
吗?为什么?
(4)该学生利用上述装置将一定质量的无水硫酸铜置于A中加热使其分解,最后测得氧
气的体积偏小,其原因可能是 (填序号)
| A.无水硫酸铜未完全分解o*m |
| B.实验结束时装置A中残留有气体 |
C.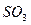 被 被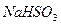 溶液吸收时产生了 溶液吸收时产生了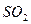 气体 气体 |
| D.最后读量筒中的读数时,E中的液面低于F中的液面 |
 出氧气的体积为224mL(标准状况)。据此可计算出二氧化硫为 mol,三氧化硫为 mol。
出氧气的体积为224mL(标准状况)。据此可计算出二氧化硫为 mol,三氧化硫为 mol。(15分)无水硫酸铜在加热条件下能发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气。某学生试图用下图所示装置来确定该化学反应中各物质的计量关系

试回答:
(1)加热过程中,试管A中发生的实验现象为 。
(2)装置E和F的作用是 ;
(3)该学生使用装置B的本意是除去混合气体中的三氧化硫以提纯氧气,他的做法正确
吗?为什么?
(4)该学生利用上述装置将一定质量的无水硫酸铜置于A中加热使其分解,最后测得氧
气的体积偏小,其原因可能是 (填序号)
A.无水硫酸铜未完全分解o*m
B.实验结束时装置A中残留有气体
C. 被
被 溶液吸收时产生了
溶液吸收时产生了 气体
气体
D.最后读量筒中的读数时,E中的液面低于F中的液面
(5)另一学生将4.8g无水硫酸铜充分加热使其完全分解后,用正确的实验方法除去了生成物中的二氧化硫和三氧化硫,最后测出氧气的体积为224mL(标准状况)。据此可计算出二氧化硫为 mol,三氧化硫为 mol。
(6)由上述实验数据可知无水硫酸铜受热分解的化学方程式为:
___________________________________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com