
题目列表(包括答案和解析)
A.1 mol甲基正离子(CH3+)所含电子数为8NA
B.标准状况下将0.5 molSO2气体与0.5 molH2S气体混合后,气体的分子总数为NA
C.500 mL 0.5 mol/L的Ca(ClO)2溶液中,含有ClO-的数目为0.5NA
D
下列离子方程式中,正确的是(? )
A.将Na2O2固体投入H218O中:2H218O+2Na2O2 = 4OH-+4Na++18O2↑
B.1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合:2AlO2- + 5 H+=Al(OH)3↓+Al3++H2O
C.碳酸氢钠溶液与少量氢氧化钡溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
D.硅酸钠溶液与醋酸溶液混合:SiO32-+ 2H+ = H2SiO3↓
(15分)
(1)下列事实中,能证明亚硫酸的酸性强于氢硫酸的是 (填字母)。
a.亚硫酸受热时易分解
b.相同条件下,等浓度的亚硫酸溶液导电能力强于氢硫酸
c.亚硫酸溶液可使品红溶液褪色,而氢硫酸不能
d.常温下,浓度均为0.k^s*5#u1mol/L的H2SO3溶液和H2S溶液的pH分别是2.k^s*5#u1和4.k^s*5#u5
(2)工业上除去高压锅用水中溶解的氧气常用的试剂有Na2SO3和N2H4(肼)。
①已知16g液态的肼与氧气反应得到氮气和液态水时,放热354.k^s*5#u87kJ,该反应的热化学方程式是 。
②除去等质量的O2,所耗Na2SO3和N2H4的质量比是 (填最简整数比)。
(3)向Na2SO3和Na2S的混合溶液中加入稀盐酸,溶液中会产生大量淡黄色沉淀。则该反应中氧化剂和还原剂的物质的量之比是 。
(4)已知Na2SO3在高温下发生分解,得到两种产物。某同学称取25.k^s*5#u2g纯净的Na2SO3·7H2O晶体在高温下隔绝空气加热至恒重,冷却后称得固体为12.k^s*5#u6g,将其完全溶于水配成1L溶液,并测溶液的pH。
①Na2SO3高温分解的化学方程式是 。
②测得溶液的pH大于0.k^s*5#u025mol/LNa2SO3溶液的pH,试解释原因(结合离子方程式说明) 。
在给定条件下,下列加点的物质在对应的化学反应中能完全耗尽的是
A.向l00. 0mL 5. 00mol/L的稀硝酸中加入5. 6 g铁
B.用40. 0 mL 10. 00mol/L的盐酸与10. 0g二氯化锰共热制取氯气
C.标准状况下,将1. 0 g铝片投入20. 0mL l8. 40mol/L的硫酸中
D.在一定条件下,用5 mol氧气和1mol二氧化硫合成三氧化硫
下图中A、B均为固体,其中B为单质。下图可用于工业生产F。回答下列问题:
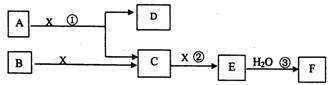
(1)A的化学式为___________________。
(2)反应①是一个氧化还原反应,该反应发生时,每生成4mol气体C,转移电子
_________________mol。
(3)写出D与铝单质反应的化学方程式______________________。
(4)反应②是可逆反应,在2L的密闭容器中投入4molC和3molX,10分钟后反应达到平衡,平衡时混合气体共6mol,则下列说法正确的是___________(填写序号字母)。
A. 工业制取F时,C和X生成E的反应是在吸收塔进行
B. 这10分钟内,X的平均反应速率是0.lmol/(L?min)
C. 当C和X的消耗速率比为2:1时,标志着反应达到平衡
D. 平衡时C的转化率是50%
E. 在工业生产中可以通过增加X浓度来提高C的转化率
F. 工业生产中直接用水来吸收E
(5)写出过量气体C与氢氧化钠溶液反应的化学方程式
_______________________________________________________。
(6)将5mL0.02mol/L的F溶液与5mL0.02mol/LNaOH溶液充分混合,若混合后溶液的体积为10mL,则混合液的pH是___________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com