
题目列表(包括答案和解析)
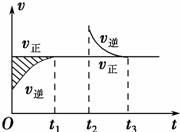 某恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
某恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )| A、Z和W在该条件下至少有一个是为气态 | B、t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量可能相等也可能不等 | C、若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等 | D、若该反应只在某温度T以上自发进行,则该反应的平衡常数K随温度升高而减小 |
三种短周期元素X、Y、Z,它们的原子序数之和为16,X、Y、Z三种元素的常见单质在常温下都是无色气体。已知X原子的最外层电子数是内层电子数的3倍,X和Y的单质直接化合形成气体A,X和Z的单质直接化合形成液态化合物B,Y和Z的单质直接化合形成的化合物C是一种无色有刺激性气味的气体。
请回答下列问题:
(1)Y元素在周期表中的位置是??????? 。
(2)C可在X的单质中燃烧得到Y的单质和化合物B,利用此反应可制成新型的化学电源(KOH溶液做电解质溶液),两个电极均由多孔碳制成,通人的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质是??????? (填物质名称);负极的电极反应式为???????????? ????????? 。
(3)C与X的单质反应生成A的化学方程式为?????????? 。
(4)常温下,C的水溶液的pH=12,则该溶液中由水电离的C(OH-)= ???? 。若向C溶液中加入等体积、等物质的量浓度的盐酸,所得溶液中水的电离程度?????? (填“大于”、“等于”或“小于”)相同条件下C溶液中水的电离程度。
(5)在2L密闭容器中放入1molC气体,在一定温度进行如下反应:
2C(g)  Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
该反应的化学平衡常数表达式是????????????? (用具体物质的化学式表示);平衡时C的转化率为???????????? 。
(6)已知:①Y2(g)+2X2(g)=2YX2(g)?  H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。
②Y2Z4(g)+X2(g)=Y2(g)+2Z2X(g)???  H=-534 kJ·mol-1。
H=-534 kJ·mol-1。
则2Y2Z4(g)+2YX2(g)=3Y2(g)+4Z2X(g)?  H=???? kJ·mol-1
H=???? kJ·mol-1
三种短周期元素X、Y、Z,它们的原子序数之和为16,X、Y、Z三种元素的常见单质在常温下都是无色气体。已知X原子的最外层电子数是内层电子数的3倍,X和Y的单质直接化合形成气体A,X和Z的单质直接化合形成液态化合物B,Y和Z的单质直接化合形成的化合物C是一种无色有刺激性气味的气体。
请回答下列问题:
(1)Y元素在周期表中的位置是 。
(2)C可在X的单质中燃烧得到Y的单质和化合物B,利用此反应可制成新型的化学电源(KOH溶液做电解质溶液),两个电极均由多孔碳制成,通人的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质是 (填物质名称);负极的电极反应式为 。
(3)C与X的单质反应生成A的化学方程式为 。
(4)常温下,C的水溶液的pH=12,则该溶液中由水电离的C(OH-)= 。若向C溶液中加入等体积、等物质的量浓度的盐酸,所得溶液中水的电离程度 (填“大于”、“等于”或“小于”)相同条件下C溶液中水的电离程度。
(5)在2L密闭容器中放入1molC气体,在一定温度进行如下反应:
2C(g) 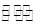 Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
 H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。 H="-534" kJ·mol-1。
H="-534" kJ·mol-1。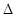 H= kJ·mol-1
H= kJ·mol-1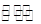 Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
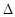 H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。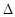 H="-534" kJ·mol-1。
H="-534" kJ·mol-1。 H= kJ·mol-1
H= kJ·mol-1 (08年北京卷)(17分)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
(08年北京卷)(17分)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y![]() Z+W
Z+W
(1)Y的电子式是_______________。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是___。
(3)用图示装置制备NO并验证其还原性。有下列主要操作:
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①步骤c后还缺少的一步主要操作是______________________。
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是_________。
③步骤c滴入稀硝酸后烧杯中的现象是______________
反应的离子方程式是_____________________________。
 (4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
①温度在T1-T2之间,反应的化学方程式是_________。
②温度在T2-T3之间,气体的平均相对分子质量是(保留1位小数)______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com