
题目列表(包括答案和解析)
X、Y、Z、W为含有10电子的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体,Z为气体.
已知:![]()
(1)X、Y、Z、W分别为________(分别写出化学式或离子符号)
(2)Y的电子式是_______________________________
(3)写出实验室制取Z的化学方程式________
(4)气体Z的收集方法是________
| ||
X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.
已知:X+Y![]() Z+W
Z+W
(1)Y的电子式是________.
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是________.
(3)用图示装置制备NO并验证其还原性.有下列主要操作:
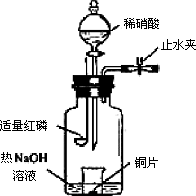
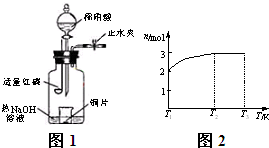
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中.
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞.
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸.
①步骤c后还缺少的一步主要操作是________.
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是________.
③步骤c滴入稀硝酸后烧杯中的现象是________.反应的离子方程式是________.
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色.温度由T1继续升高到T2的过程中,气体逐渐变为无色.若保持T2,增大压强,气体逐渐变为红棕色.气体的物质的量n随温度T变化的关系如图所示.
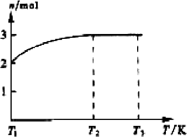
①温度在T1T2之间,反应的化学方程式是________.
②温度在T2T3之间,气体的平均相对分子质量是(保留1位小数)________.
Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.已知:X+Y![]() Z+W
Z+W
(1)Y的电子式是________.
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是________.
(3)用下图示装置制备NO并验证其还原性.有下列主要操作:
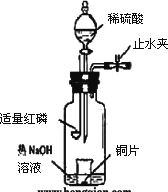
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中.
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞.
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸.
①步骤c后还缺少的一步主要操作是________.
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是________.
③步骤c滴入稀硝酸后烧杯中的现象是________.反应的离子方程式是________.
)X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,一般情况下X的单质只有氧化性。
(1)写出实验室制取W2反应的离子方程式 。
(2)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究YX2和W2的性质。
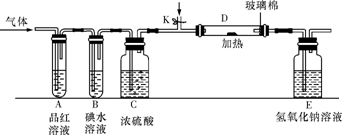
①分别通入YX2和W2,在装置A中观察到的现象是否相同(填“相同”或“不相同”) ;若装置D中装的是铁粉,当通入W2时D中观察到的现象为 ;若装置D中装的是五氧化二钒,当通入YX2时,打开K通入适量X2,化学反应方程式为 ;
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,则该反应的化学方程式为 。
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量(填字母) ,可以看到白色沉淀生成。
A.氨水 B.稀盐酸
C.稀硝酸 D.氯化钙
(4)若由元素Y和X组成-2价酸根Z,Z中Y和X的质量比为Y∶X=4∶3,当W2与含Z的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出W2与Z的溶液完全反应产生浅黄色沉淀的离子方程式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com