
题目列表(包括答案和解析)
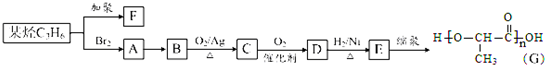


| H2O |
| △ |
| H2O |
| △ |
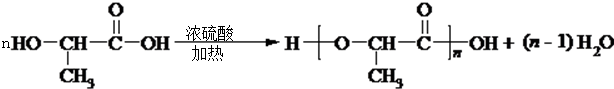
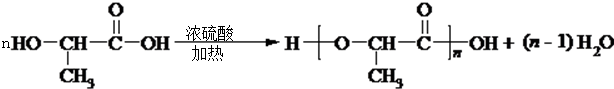
| A、①③④②⑤ | B、①④⑤③② | C、⑤④①③② | D、⑤①③④② |
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 |
| 3.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 1.5mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
| 3.0mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
反应进程 酸 | 1 min | 2 min | 5 min | 15 min | 20 min |
3 mol·L-1HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
1.5 mol·L-1H2SO4 | 均无明显现象(无气泡) | ||||
3 mol·L-1H2SO4 | 均无明显现象(无气泡) | ||||
无论是用1.5 mol·L-1还是用3 mol·L-1的稀硫酸,均无明显现象。其结论还是与教材的叙述不相符合。
(1)为了探究“铝跟稀盐酸、稀硫酸反应的差异原因”,你能对问题的答案作出哪些假设(或猜想)?
假设一:______________________________________________________________。
假设二:______________________________________________________________。
……
(2)为了论证上述假设,你设计的实验方案是:(探究过程)
_____________________________________________________________________。
实验用品:仪器(略,凡是实验需要的都有)。?
药品:3.0 mol·L-1盐酸,1.5 mol·L-1硫酸,3.0 mol·L-1硫酸、相同大小的铝片(纯度>99.5%)。
实验过程:往3支相同的试管中分别加入相同的铝片各一片,再往试管中分别加入等体积的3.0 mol·L-1盐酸、1.5 mol·L-1硫酸、3.0 mol·L-1硫酸。观察反应进行到1、2、5、15、20 min时的铝与酸反应的情况,结果如下:
反应进程/min | 1 | 2 | 5 | 15 | 20 |
3.0 mol·L-1盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
1.5 mol·L-1硫酸 | 均无明显现象(无气泡产生) | ||||
3.0 mol·L-1硫酸 | 均无明显现象(无气泡产生) | ||||
通过上述实验可知,无论是用1.5 mol·L-1硫酸还是3.0 mol·L-1硫酸,均无明显的现象。而3.0 mol·L-1盐酸与铝片反应的现象却十分明显。?
问题1:为了探究“铝与稀盐酸和稀硫酸反应差异的原因”,你能对问题的答案作出哪些假设或猜想(列出两种即可)??
假设一: ,?
假设二: 。?
问题2:为了验证上述假设,你设计的实验方案是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com