
题目列表(包括答案和解析)
 金属及其化合物在人类生活、生产中发挥着重要的作用.
金属及其化合物在人类生活、生产中发挥着重要的作用.金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)将一小块金属钠投入盛有水的烧杯中,发生反应的化学方程式为 :
(2)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是 (填化学式,下同);适宜做耐火材料的是 ;
(3)金属铝既能与盐酸反应,又能与烧碱溶液反应,请写出金属铝与烧碱溶液反应的离子方程式: 。
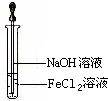
(4)取少量FeCl2溶液,按图所示操作,使其跟NaOH溶液反应。 可观察到试管中出现白色絮状沉淀,继而变成灰绿色,最后变成红褐色,请写出与上述现象相关的反应的化学方程式: 、 。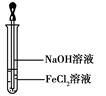
(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 (填序号)。
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |
金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)将一小块金属钠投入盛有水的烧杯中,发生反应的化学方程式为 :
(2)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是 (填化学式,下同);适宜做耐火材料的是 ;
(3)金属铝既能与盐酸反应,又能与烧碱溶液反应,请写出金属铝与烧碱溶液反应的离子方程式: 。
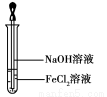
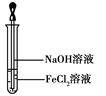
(4)取少量FeCl2溶液,按图所示操作,使其跟NaOH溶液反应。 可观察到试管中出现白色絮状沉淀,继而变成灰绿色,最后变成红褐色,请写出与上述现象相关的反应的化学方程式: 、 。
(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 (填序号)。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com