СОДаКЗВИјо№ӨТөЦРөД·ПФьЈ¬ЦчТӘә¬УРГҫЎўМъЎўВБЎўёЖөИөД№иЛбСОәНМјЛбСОЈ®КөСйКТТФСОДаОӘФӯБПЦЖИЎMgSO
4?7H
2OөДКөСй№эіМИзПВЈә

ТСЦӘЈәўЩKsp[MgЈЁOHЈ©
2]=6.0ЎБ10
-12Ј®ўЪFe
2+ЎўFe
3+ЎўAl
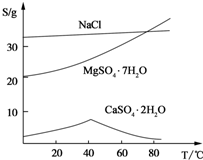
3+ҙУҝӘКјіБөнөҪіБөнНкИ«өДpH·¶О§ТАҙООӘЈә7.1Ў«9.6Ўў2.0Ў«3.7Ўў3.1Ў«4.7Ј®ўЫИэЦЦ»ҜәПОпөДИЬҪв¶ИЈЁSЈ©ЛжОВ¶Иұд»ҜөДЗъПЯИзПВНјЛщКҫЈ®

ЈЁ1Ј©ФЪСОДаЦРјУИлПЎБтЛбөчpHОӘ1Ў«2ТФј°өЪТ»ҙОЦу·РөДДҝөДКЗ
МбёЯMg2+өДҪюИЎВК
МбёЯMg2+өДҪюИЎВК
ЈЁ2Ј©ИфИЬТәЦРMg
2+өДЕЁ¶ИОӘ6.0mol?L
-1Ј¬ФтИЬТәpHЎЭ
8
8
ІЕҝЙДЬІъЙъMgЈЁOHЈ©
2іБөнЈ®
ЈЁ3Ј©өЪ¶юҙО№эВЛРиТӘіГИИҪшРРЈ¬ЦчТӘФӯТтКЗ
ОВ¶ИҪПёЯКұёЖСОУлГҫСО·ЦАлөГёьі№өЧЈЁ»тёЯОВПВCaSO4?2H2OИЬҪв¶ИРЎөИәПАнҙр°ёҫщҝЙЈ©
ОВ¶ИҪПёЯКұёЖСОУлГҫСО·ЦАлөГёьі№өЧЈЁ»тёЯОВПВCaSO4?2H2OИЬҪв¶ИРЎөИәПАнҙр°ёҫщҝЙЈ©
Ј¬ЛщөГВЛФьөДЦчТӘіЙ·ЦКЗ
AlЈЁOHЈ©3ЎўFeЈЁOHЈ©3ЎўCaSO4?2H2O
AlЈЁOHЈ©3ЎўFeЈЁOHЈ©3ЎўCaSO4?2H2O
Ј®
ЈЁ4Ј©ҙУВЛТәўтЦР»сөГMgSO
4?7H
2Oҫ§МеөДКөСйІҪЦиТАҙООӘЈәўЩПтВЛТәўтЦРјУИл
NaOHИЬТә
NaOHИЬТә
Ј»ўЪ№эВЛЈ¬өГіБөнЈ»ўЫ
ПтіБөнЦРјУЧгБҝПЎБтЛб
ПтіБөнЦРјУЧгБҝПЎБтЛб
Ј»ўЬХф·ўЕЁЛхЈ¬ҪөОВҪбҫ§Ј»ўЭ№эВЛЎўПҙөУөГІъЖ·Ј®
ЈЁ5Ј©Иф»сөГөДMgSO
4?7H
2OөДЦКБҝОӘ24.6gЈ¬ФтёГСОДаЦРГҫ[ТФMgЈЁOHЈ©
2јЖ]өД°Щ·Цә¬БҝФјОӘ
20.0%
20.0%
ЈЁMgSO
4?7H
2OөДПа¶Ф·ЦЧУЦКБҝОӘ246Ј©Ј®