
题目列表(包括答案和解析)
 2NH3(g).在一体积为10L且容积不变的密闭容器中放入1mol N2和3mol H2 ,在一定条件下发生反应,经4min达到化学平衡状态,测得容器中氨气的物质的量为0.6mol.。求:
2NH3(g).在一体积为10L且容积不变的密闭容器中放入1mol N2和3mol H2 ,在一定条件下发生反应,经4min达到化学平衡状态,测得容器中氨气的物质的量为0.6mol.。求:若定义某物质的转化率为消耗掉的该物质的物质的量占起始时该物质的原物质的量的百分比。已知合成氨反应为N2(g) + 3H2(g) ![]() 2NH3(g).在一体积为10L且容积不变的密闭容器中放入1mol N2和3mol H2 ,在一定条件下发生反应,经4min达到化学平衡状态,测得容器中氨气的物质的量为0.6mol.。求:
2NH3(g).在一体积为10L且容积不变的密闭容器中放入1mol N2和3mol H2 ,在一定条件下发生反应,经4min达到化学平衡状态,测得容器中氨气的物质的量为0.6mol.。求:
(1)氮气的转化率
(2)用氢气表示平均反应速率是多少?
(3)平衡状态时氢气的物质的量浓度。
HO—CH2—CH2—OH![]()
HO—CH2CH2—O—CH2CH2—OH![]()
HO—CH2CH2—O—CH2CH2—O—CH2CH2OH ![]()
(1)以![]() 的形式表示上述一系列醇醚的结构简式:__________________。
的形式表示上述一系列醇醚的结构简式:__________________。
(2)写出上述同系列的分子式通式:________________
(3)推算该同系列化合物中碳元素的质量分数最大值为__________________。
(12分)测定平衡常数对定量认识化学反应具有重要意义。已知:I2能与I-反应成
I3-,并在溶液中建立如下平衡:I2 +I- I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。
I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。
I、某同学为测定上述平衡体系中c(I2),采用如下方法:取V1 mL平衡混合溶液,用c mol·L-1的Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗V2 mL的Na2S2O3溶液。根据V1、V2和c可求得c(I2)。
(1)上述滴定时,可采用_________做指示剂,滴定终点的现象是________。
(2)下列对该同学设计方案的分析,正确的是__________(填字母)。
A.方案可行。能准确测定溶液中的c(I2)
B.不可行。因为I-能与Na2S2O3发生反应
C.不可行。只能测得溶液中c(I2)与c(I3-)之和
Ⅱ、化学兴趣小组对上述方案进行改进,拟采用下述方法来测定该反应的平衡常数(室温条件下进行,溶液体积变化忽略不计):
已知:①I-和I3-不溶于CCl4;②一定温度下碘单质在四氯化碳和水混合液体中,碘单质的浓度比值即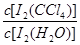 是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
(3)操作Ⅰ使用的玻璃仪器中,除烧杯、玻璃棒外,还需要的仪器是______(填名称)。
试指出该操作中应注意的事项为 。(任写一条)
(4)下层液体中碘单质的物质的量浓度是__________。
(5)实验测得上层溶液中c(I3-)="0.049" mol·L-1,结合上述有关数据,计算室温条件下反应I2+I- I3-的平衡常数K=__________(用具体数据列出计算式即可)。)
I3-的平衡常数K=__________(用具体数据列出计算式即可)。)
 I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。
I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。
 是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题: I3-的平衡常数K=__________(用具体数据列出计算式即可)。
I3-的平衡常数K=__________(用具体数据列出计算式即可)。 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com