
题目列表(包括答案和解析)
资料:(1)草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色;(2)KMnO4在酸性条件的还原产物为Mn2+。某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究。
(1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成。这说明草酸亚铁晶体具有 (填“氧化性”、“还原性”或“碱性”)。若反应中消耗1 mol FeC2O4·2H2O,则参加反应的KMnO4为 ______mol。
(2)资料表明:在密闭容器中加热到一定温度时,草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体。课题组根据课本上所介绍的铁的氧化物的性质,对黑色固体的组成提出如下假设,请你完成假设二和假设三:
假设一:全部是FeO;假设二: ;假设三:
(3)为验证上述假设一是否成立,课题组进行如下研究。
【定性研究】请你完成下表中内容。
|
实验步骤(不要求具体的操作过程) |
预期实验现象和结论 |
|
取少量黑色固体, |
|
【定量研究】课题组在文献中查阅到,FeC2O4·2H2O受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,FeC2O4·2H2O晶体受热分解的化学方程式为: 。
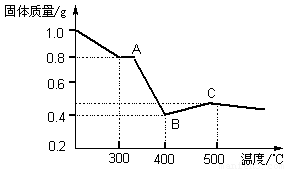
根据图象,如有1.0 g草酸亚铁晶体在坩埚中敞口充分加热,最终残留黑色固体的质量大于0.4 g。某同学由此得出结论:假设一不成立。你是否同意该同学的结论 (填“同意”或“不同意”),并简述理由 。
⑴ 写出四种化合物的化学式:
A. ; B. ; C. ; D. 。
⑵ 写出有关化学反应方程式:
a. A在空气中燃烧: ,
b. B与氢卤酸反应: ,
c. D与水反应: 查看答案和解析>>
阅读、分析下列两个材料:
材料一
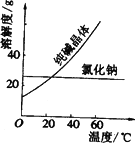
材料二
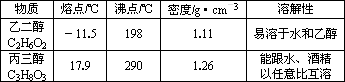
根据上述材料及课本知识,回答下列问题(填写序号):
A.蒸馏法
B.萃取法
C.“溶解、结晶、过滤”的方法
D.分液法
E.层析
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用________,
(2)将乙二醇和丙三醇相互分离的最佳方法是________,
(3)用CCl4提取溴水中的溴单质的最佳方法是________,
(4)分离汽油和水的最佳方法是________.
A、B、C、D四种化合物均为中学课本中常见的物质,它们的化学式都符合RX2型,且其中所含元素的原子结构均达8电子结构。组成这四种化合物中的元素的原子序数都不超过20.构成这四种化合物的化学键为:C只有离子键,D既有离子键又有非极性共价键。A,B只有共价键,A的熔点很低,B的熔点却很高。A和C都难与各种氢卤酸反应;B、C都难溶于水。D却与水剧烈反应,所产生的气体是一种烃。A能在空气里燃烧,B、C、D则不能。B可与某种氢卤酸反应,所产生的气体不能燃烧。根据上述进行判断:
⑴ 写出四种化合物的化学式:
A. ; B. ; C. ; D. 。
⑵ 写出有关化学反应方程式:
a. A在空气中燃烧: ,
b. B与氢卤酸反应: ,
c. D与水反应: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com