
题目列表(包括答案和解析)
实验室中通常加热无水乙醇与浓硫酸的混合物的方法制取乙烯,浓硫酸的作用是乙醇反应的催化剂和吸水剂.在具体的化学实验中常因加热的温度过高导致副反应发生而使乙烯气体中混有二氧化硫气体.如图所表示的装置可以用于确认乙烯气体中混有二氧化硫气体.可选择的化学试剂有:

A.品红溶液 B.烧碱溶液 C.浓硫酸 D.酸性高锰酸钾溶液
回答下列问题:
(1)由乙醇生成乙烯的化学反应方程式是________,该化学反应所属的类型可以是________或________.
A.取代反应 B.加成反应 C.脱水反应 D.分解反应
(2)图中①、②、③、④的容器内盛放的化学试剂分别是(填写代号)
①________、②________、③________、④________.
(3)能说明二氧化硫气体存在的现象是________.
(4)使用装置②的目的是________;使用装置③的目的是________.
(5)确认乙烯气体存在的现象是________.
(6)实验室中可以采用将乙烯气体通入酸性高锰酸钾溶液的实验方法证明乙烯具有容易被氧化的化学性质.在将乙烯气体通入酸性高锰酸钾溶液之前要进行的一项实验是________.
(14分)实验题:某班级的探究小组研究氧化铜能否在氯酸钾的受热分解中起到催化剂的作用,设计了如下实验:
(一) 制备氧化铜
(1)称取5.0gCuSO4·5H2O晶体,研细后溶解:此步骤需要的仪器有________________________。
(2)向盛有硫酸铜溶液的烧杯中滴加NaOH溶液,直到不再产生沉淀为止。此步实验现象:____________;离子方程式为:_________________。
(3)A.把步骤(2)中的溶液和沉淀转移到蒸发皿内,稍微加热至沸腾,搅拌,直到沉淀全部变为黑色固体,停止加热,再过滤、洗涤、干燥、再转移到研钵中研细备用。
B.把步骤(2)中的溶液和沉淀转移到过滤器中过滤,洗涤,将上述沉淀在蒸发皿中进行蒸发,至全部变为黑色固体为止。再转移到研钵中研细备用。
你认为那一个步骤更好,说明理由:______________________。
(二) 证明氧化铜起催化剂作用
设计对比实验①任取两份氯酸钾,分别放入两支试管,在其中一份中加入经精确称量的ng氧化铜粉末;②将两份氯酸钾同时在相同条件下正确加热,将放出的气体通入水中;③停止加热,冷却,将原先混有氧化铜的反应后混合物加水溶解,小心过滤,得到滤出物,洗涤并干燥;④观察滤出物的颜色和状态;⑤将滤出物和炭粉混和,在密闭容器中高温加热,将反应产生的气体通入澄清的石灰水中,并观察试验现象。
请回答下列问题:
(1)氧化铜作催化剂的理论依据是:_____________________。
(2)以上实验步骤,有一步不够严密,请指出是那一步:______(填步骤序号);该步骤应该做何改进?__________________。
(3)要达到实验目的,还应该再增加一个实验步骤,这个实验步骤是______。
(4)若用另一套实验装置和操作替换第⑤步实验,也可以达到这一步的实验目的,请从图中所给的仪器作出合理选择,将它们连接成一个符合设计者要求的试验装置。
这个实验装置按照气流从左到右的连接顺序是__接__接__接__接__接__。
反应进程 酸 | 1 min | 2 min | 5 min | 15 min | 20 min |
3 mol·L-1HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
1.5 mol·L-1H2SO4 | 均无明显现象(无气泡) | ||||
3 mol·L-1H2SO4 | 均无明显现象(无气泡) | ||||
无论是用1.5 mol·L-1还是用3 mol·L-1的稀硫酸,均无明显现象。其结论还是与教材的叙述不相符合。
(1)为了探究“铝跟稀盐酸、稀硫酸反应的差异原因”,你能对问题的答案作出哪些假设(或猜想)?
假设一:______________________________________________________________。
假设二:______________________________________________________________。
……
(2)为了论证上述假设,你设计的实验方案是:(探究过程)
_____________________________________________________________________。
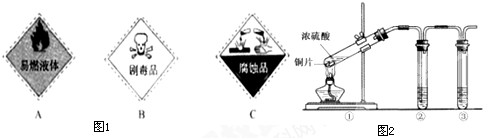
(15分)硫酸是一种实验室常用的化学试剂。请按要求填空:
(1)浓硫酸试剂瓶上适合贴上的图标是 (填写字母标号)。
(2)实验室有1.00mol·L-1的硫酸溶液,从中准确量出10.00 mL,其物质的量浓度为 mol·L-1。现将准确量出的10.00mL的硫酸溶液配制成0.100mol·L-1的稀硫酸,所需要的玻璃仪器除烧杯、玻璃棒还需 和 。在配制过程中定容时俯视,则所配溶液浓度 (填“偏大”或“偏小”或“无影响”)
(3)用右上图所示的实验装置②验证铜与浓硫酸反应生成的气体产物,则装置②、③中试剂依次为下列的 和
A.品红溶液 B.BaCl2溶液 C.NaOH溶液 D.AgNO3溶液
(4)装置①中发生反应的化学方程式为 若装置①中加入铜6.4g和含有0.2molH2SO4的浓硫酸,则产生二氧化硫质量
A. 等于6.4克 B.大于6.4克 C.小于6.4克 D.不能确定
(5)若将装置①中的铜片换成木炭,装置②试管内为氢硫酸溶液, 装置③试管内为澄清石 灰水,则装置①中发生反应的化学方程式为 。装置②中主要反应的氧化剂和还原剂物质的量之比是 。根据装置③观察到有白色沉淀生成的现象 (填“能”或“不能”)判断该白色沉淀一定只有CaCO3。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com