某兴趣小组的同学为了探究化学反应前后反应物与生成物之间的质量关系设计了如下三个实验:
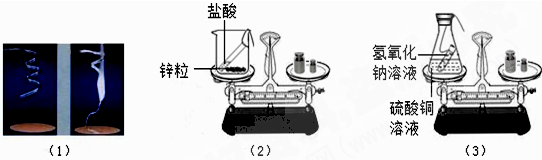
实验①:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量
实验②:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.
(化学方程式是:Zn+2HCl=ZnCl
2+H
2↑)
实验③:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.化学方程式是:CuSO
4+2NaOH=Cu(OH)
2↓+Na
2SO
4他们得到三次实验的数据见下表:
| 编号 |
实验① |
实验② |
实验③ |
| 反应前/g |
4.8 |
112.6 |
118.4 |
| 反应后/g |
8.0 |
112.4 |
118.4 |
(1)在实验①中反应后的质量比反应前明显增加了,请解释原因:
(2)由上表中数据分析可知实验①中参加反应的氧气质量为
,实验②中生成氢气的质量为
.
(3)在上述三个实验中都
(填“遵循”或者“不遵循”)质量守恒定律,但只有实验
能正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有
时,必须在
进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:
.
(5)在化学反应前后,肯定不会变化的是
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积 ⑦物质的状态.

