
题目列表(包括答案和解析)
(10分)某活动课程小组拟用50 mLNaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入过量的CO2气体生成NaHCO3,设计了如下实验步骤:
a.取25 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
b.小火煮沸溶液1~2 min,赶走溶解在溶液中的CO2气体;
c.在得到的溶液中加入另一半(25 mL)NaOH溶液,使其充分混合反应.
(1)此方案能制得较纯净的Na2CO3,写出c步骤的离子方程式_________________.
此方案第一步的实验装置如下图所示:
(2)加入反应物前,如何检验整个装置的气密性:________________________ ________________________________________________
(3)若用大理石与盐酸制CO2,则装置B中盛放的试剂是_____ _,作用是_____________________________________________
(4)在实验室通常制法中,装置A还可作为下列______ (填序号)气体的发生装置.
①HCl ②H2 ③O2 ④NH3
(5)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g/mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_______ mol/L.
(10分)某活动课程小组拟用50 mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入过量的CO2气体生成NaHCO3,设计了如下实验步骤:
a.取25 mL  NaOH溶液吸收过量的CO2气体,至CO2
NaOH溶液吸收过量的CO2气体,至CO2 气体不再溶解;
气体不再溶解;
b.小火煮沸溶液1~2 min,赶走溶解在溶液中的CO2气体;
c.在得到的溶液中加入另一半(25 mL)NaOH溶液,使其充分混合反应.
(1)此方案能制得较纯净的Na2CO3,写出c步骤的离子方程式_________________.
此方案第一步的实验装置如下图所示:
(2)加入反应物前,如何检验整个装置的气密性:________________________ ________________________________________________
(3)若用大理石与盐酸制CO2,则装置B中盛放 的试剂是_____
的试剂是_____  _,作用是_____________________________________________
_,作用是_____________________________________________
(4)在实验室通常制法中,装置A还可作为下列______ (填序号)气体的发生装置.
①HCl ②H2 ③O2 ④NH3
(5)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g/mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_______ mol/L.
(10分)某活动课程小组拟用50 mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入过量的CO2气体生成NaHCO3,设计了如下实验步骤:
a.取25 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
b.小火煮沸溶液1~2 min,赶走溶解在溶液中的CO2气体;
c.在得到的溶液中加入另一半(25 mL)NaOH溶液,使其充分混合反应.
(1)此方案能制得较纯净的Na2CO3,写出c步骤的离子方程式_________________.
此方案第一步的实验装置如下图所示:
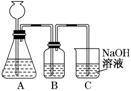
(2)加入反应物前,如何检验整个装置的气密性:________________________ ________________________________________________
(3)若用大理石与盐酸制CO2,则装置B中盛放的试剂是_____ _,作用是_____________________________________________
(4)在实验室通常制法中,装置A还可作为下列______ (填序号)气体的发生装置.
①HCl ②H2 ③O2 ④NH3
(5)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g/mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_______ mol/L.
 NaOH溶液吸收过量的CO2气体,至CO2
NaOH溶液吸收过量的CO2气体,至CO2 气体不再溶解;
气体不再溶解;
 的试剂是_____
的试剂是_____  _,作用是_____________________________________________
_,作用是_____________________________________________碘化钠是常用的分析试剂,还用于医疗、照相业。工业上用铁屑还原法制备NaI,其主要流程如下,请回答问题:
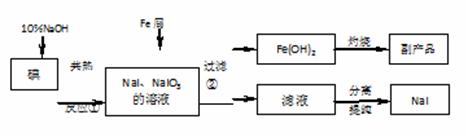
已知:NaI易被空气氧化;反应②为:3Fe + IO3-+ 3H2O → 3Fe (OH)2 ↓ +I-
40.实验室灼烧Fe(OH)2主要在 进行(填仪器名称);灼烧后的副产品是 __________(写化学式)。
41.判断①中碘单质是否完全反应的实验方法是 ;
42.实验室配制一定量10%NaOH溶液,其操作步骤是 。
43.测定产品中NaI含量的方法是:
a.称取3.000 g样品、溶解,在250 mL容量瓶中定容;
b.量取25.00 mL待测溶液于锥形瓶中;
c.用0.1000 mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为19.00 mL。
①测定过程所需仪器在使用前需要检查是否漏液的有 。
② 该样品中NaI的质量分数为 。
③ 若测定结果偏低,试分析可能的原因(任写两条):
、 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com