
题目列表(包括答案和解析)
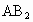 离子化合物的阴、阳离子的电子层结构相同,每摩
离子化合物的阴、阳离子的电子层结构相同,每摩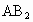 分子中含有54摩电子,根据下列反应:①
分子中含有54摩电子,根据下列反应:① ②
②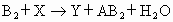 ③
③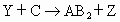 (Z有漂白作用)
(Z有漂白作用)
(1)写出下列物质的化学式: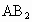 ______X_______Y_______Z________
______X_______Y_______Z________
(2)用电子式表示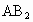 的形成过程________________________________.
的形成过程________________________________.
(3)写出反应②的化学方程式_____________________________________.
![]() 离子化合物的阴、阳离子的电子层结构相同,每摩
离子化合物的阴、阳离子的电子层结构相同,每摩![]() 分子中含有54摩电子,根据下列反应:
分子中含有54摩电子,根据下列反应:
①![]()
②![]() +X→Y+
+X→Y+![]()
③Y+C→![]() +Z Z有漂白作用.
+Z Z有漂白作用.
(1)写出下列物质的化学式![]() ________.
________.
X________,Y________,Z________.
(2)用电子式表示![]() 的形成过程________.
的形成过程________.
(3)写出反应②的化学方程式________.
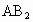 离子化合物的阴、阳离子的电子层结构相同,每摩
离子化合物的阴、阳离子的电子层结构相同,每摩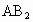 分子中含有54摩电子,根据下列反应:①
分子中含有54摩电子,根据下列反应:①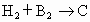 ②
②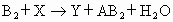 ③
③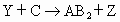 (Z有漂白作用)
(Z有漂白作用)
(1)写出下列物质的化学式: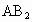 ______X_______Y_______Z________
______X_______Y_______Z________
(2)用电子式表示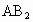 的形成过程________________________________.
的形成过程________________________________.
(3)写出反应②的化学方程式_____________________________________.
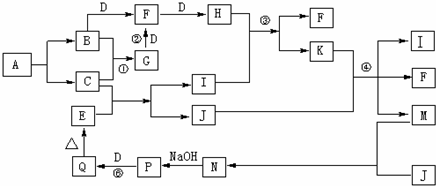
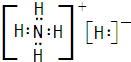
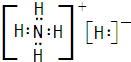
| ||
| ||
①H2+B2![]() C
C
②B2+X![]() Y+AB2+H2O
Y+AB2+H2O
③Y+C![]() AB2+Z Z漂白作用
AB2+Z Z漂白作用
(1)写出下列物质的化学式:AB2_____________,X____________,Y___________,Z_________。
(2)用电子式表示AB2的形成过程:_________________________________________________。
(3)写出反应②的化学方程式:_____________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com