
题目列表(包括答案和解析)
|
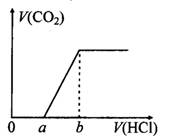
2.7 g铝粉分别与体积均为100 mL、浓度均为2 mol/L的①硫酸溶液、②烧碱溶液、③盐酸完全反应,放出氢气的体积(相同条件)是 | |
| [ ] | |
A. |
①=②=③ |
B. |
①=②>③ |
C. |
①>②>③ |
D. |
②>①=③ |
50 ml 1.0 mol·L-1盐酸与50 mL 1.1 mol·L-1 NaOH溶液在如下图1所示的装置中进行中和反应.通过测定反应过程中放出的热量计算中和热.回答下列问题:

①从实验装置上看,大烧杯上没有________,会导致求得的中和热数值________(填“偏大”“偏小”或“无影响”);实验装置中也缺少环形玻璃搅拌棒,若用环形铜质搅拌棒代替,会导致求得的中和热数值________(填“偏大”“偏小”或“无影响”).
②若实验中分多次把NaOH溶液倒入盛有盐酸的小烧杯中,则求得的中和热数值________(填“偏大”“偏小”或“无影响”)
③若实验中改用60 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”),该实验中NaOH溶液的浓度大于盐酸浓度的作用是________.
④若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会________(填“偏大”“偏小”或“无影响”).
⑤当室温低于10℃时进行实验,对实验结果会造成较大误差,其原因是________.
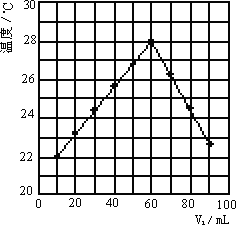
⑥若将V2mL未知浓度的NaOH溶液,加入内盛有V1mL 1.0 mol/L HCl溶液的小烧杯中混合均匀后测量并记录溶液温度,且每次实验中均保持V1+V2=100 mL,实验结果如下图2所示(以温度为纵坐标,V1为横坐标).做该实验时环境温度________22℃(填<、=、>),NaOH溶液的浓度约为________mol/L
50 mL 1.0 mol·L-1盐酸与50 mL 1.1 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量计算中和热.回答下列问题:

(1)从实验装置上看,大烧杯上没有________,会导致求得的中和热数值________(填“偏大”“偏小”或“无影响”);实验装置中还缺少环形玻璃搅拌棒,也会导致求得的中和热数值________(填“偏大”“偏小”或“无影响”);其中环形玻璃搅拌棒的作用为________.
(2)若实验中分多次把NaOH溶液倒入盛有盐酸的小烧杯中,则求得的中和热数值________(填“偏大”“偏小”或“无影响”).
(3)若实验中改用60 mL 1.0 mol·L-1盐酸跟60 mL 1.1 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”).
(4)若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会________(填“偏大”“偏小”或“无影响”).
(5)若将V2 mL未知浓度的NaOH溶液加入盛有V1 mL 1.0 mol/L HCl溶液的小烧杯中,混合均匀后测量并记录溶液温度,且每次实验中均保持V1+V2=100 mL,实验结果如图所示(以温度为纵坐标,V1为横坐标).做该实验时起始环境温度________22℃(填<、=、>),NaOH溶液的浓度约为________mol/L.
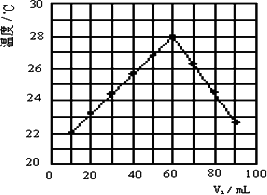
(1)常温下,0.1 mol/L的醋酸和0.1mol/L的盐酸各100 mL,分别与足量的锌粒反应,产生的气体体积前者 后者(填“<”、“>”或“=”).
(2)在25℃条件下将pH=5的氯化铵溶液稀释100倍,稀释后溶液的pH为(填选项字母,下同) .
A.5 B.7 C.3~5之间 D.5~7之间
(3)将体积和物质的量浓度都相同的醋酸和氢氧化钠溶液混合后,溶液呈 性(填“酸”,“中”或“碱”,下同),溶液中c(Na+) c(CH3COO-)(填“ >” 或“=”或“<”,下同 )。
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性,溶液中c(Na+) c(CH3COO-)
(5)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+) 氢氧化钠溶液中c(OH-),m与n的大小关系是m n。
(6)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是 。(多选、错选不得分)
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质;
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
E.未用标准液润洗碱式滴定管。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com