
题目列表(包括答案和解析)
| 实验编号 | T/K | KMnO4浓度 /mol?L-1 |
H2C2O4浓度 /mol?L-1 |
实验目的 |
| ① | 298 | 0.01mol?L-1 | 0.1mol?L-1 | 为以下实验做对照 |
| ② | 323 323 |
0.01 mol?L-1 0.01 mol?L-1 |
0.1 mol?L-1 0.1 mol?L-1 |
探究温度对反应速率的影响 探究温度对反应速率的影响 |
| ③ | 298 298 |
0.01 mol?L-1 0.01 mol?L-1 |
0.2 mol?L-1 0.2 mol?L-1 |
探究浓度对反应速率的影响 |


| 化学式 | Ca(OH)2 | CaSO4 | BaCO3 | BaSO4 | MgCO3 | Mg(OH)2 |
| Ksp | 1.0×10一4 | 7.1×10一5 | 8.1×10一9 | 1.08×10一10 | 3.5×10一5 | 1.6×10一11 |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
氯化铵溶液呈酸性 NH |
B. |
氢硫酸电离 H2S |
C. |
向小苏打溶液中加入醋酸溶液 HCO |
D. |
在标准状况下,向10 mL 0.1 mol·L-1 FeBr2溶液中通入22.4 mL Cl2 2Fe2++2Br-+2Cl2 |
A.3∶2∶2 B.1∶2∶3?
C.1∶3∶3 D.3∶1∶1?
(12分)实验室常用准确称量的邻苯二甲酸氢钾(结构简式如图所示)来准确测定NaOH标准溶液的浓度,即分析化学实验中常称为“标定”的一种方法。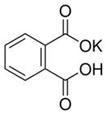
已知:①NaOH溶液的浓度在0.1 mol·L-1左右,滴定终点时溶液的pH应为9.1。
②邻苯二甲酸氢钾相对分子质量为204
(1)写出邻苯二甲酸氢钾与NaOH反应的离子方程式________________________。
(2)将用托盘天平称好的邻苯二甲酸氢钾放于锥形瓶中,加适量的水溶解,溶液呈无色,
再加入指示剂______(从甲基橙、酚酞中选择),用NaOH溶液滴定到终点时,现象是____________。
某学生进行了四次实验,实验数据如下表:
| 实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
| 1 | 0.4080 | 18.20 |
| 2 | 17.10 | |
| 3 | 16.90 | |
| 4 | 17.00 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com