
题目列表(包括答案和解析)
I.下面是几种实验中常用的仪器:
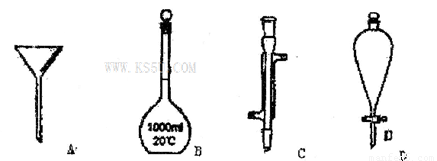
写出序号所代表的仪器的名称:
A____________;B____________;C_____________;D______________.
Ⅱ.实验室要配制480 mL, O.2 mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有___________(填选项的字母)。
A.烧杯 B.500 mL容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为_______________g。
(3)取用任意体积的该NaOH溶液时,下列物理量中不随所取体积的多少而变化的是________________________。
A.溶液中NaOH的物质的量 B.溶液的浓度
C.溶液中的数目 D.溶液的密度
(4)在配制上述溶液的过程中,下列情况对NaOH溶液物质的量浓度有何影响(填”偏高”、”偏低”、或”无影响”)

①未经冷却趁热将溶液注入容量瓶中:__________________。
②容量瓶用蒸馏洗涤后残留有少量的水:_______________。
③定容时某同学观察液面的情况如图所示,则所配置的溶液的浓_______________。
④转移溶液后,未洗涤烧杯和玻璃棒就直接定容______________。

②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是________________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了_________________。定容,摇匀。将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度
(6)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会__________(填“偏高”、“偏低”或“无影响”)。
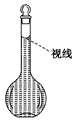
实验室需要配制0.50 mol/L NaCl溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、________、________以及等质量的几片滤纸。
(2)计算。配制该溶液需取NaCl晶体的质量为________g。
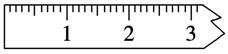 (3)称量。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在右图中用一根竖线标出游码左边缘所处的位置:
②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解。该步实验中需要使用玻璃棒,目的是_______________________________。
(5)转移、洗涤。在转移时应使用________引流,洗涤烧杯2~3次是____________________。
(6)定容,摇匀。
(7)在配制溶液(或者稀释浓溶液)的过程中,存在引起误差的一些错误操作,可能造成所配溶液的浓度会受到影响,请完成下表(在空格处填偏大、偏小或者无影响)。
| 引起误差的一些错误操作 | 对CB的影响 |
| 定容时,俯视刻度线 | |
| 转移溶液时,玻璃棒下端靠在容量瓶刻度线以上 | |
| 洗涤量取浓溶液的量筒并将洗涤液转移到容量瓶 | |
| 定容后,经振荡、摇匀、静置、液面低于刻度线再加水 |
实验室里需要配制480 mL 0.10 mol·L-1的硫酸铜溶液,下列实验方案及实验操作正确的是________

实验室欲配制
480 mL 0.1 mol/L Na2CO3溶液.(1)应该用托盘天平称取无水碳酸钠粉末________g.
(2)若在称量样品时,药品放在天平的右盘,砝码放在天平的左盘,天平平衡时,实际称量的碳酸钠粉末是________g(1 g以下用游码).
(3)配制Na2CO3溶液时需要使用的主要仪器有________________.
(4)下列情况会使所配溶液浓度偏低的是________.
①称取的碳酸钠中带有部分结晶水
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com