
题目列表(包括答案和解析)
工业品纯碱中常含有少量的NaCl等杂质,图中的仪器装置可用来测定纯碱中![]() 的质量分数,图中标号:①空气,②某溶液,③纯碱样品,④稀
的质量分数,图中标号:①空气,②某溶液,③纯碱样品,④稀 ,⑤浓
,⑤浓 ,⑥碱石灰,⑦碱石灰.
,⑥碱石灰,⑦碱石灰.

实验步骤是:
①检查装置的气密性;
②准确称量盛有碱石灰干燥管Ⅰ的质量(设为 );
);
③准确称量一定量的纯碱的质量(设为 ),并将其放入广口瓶中;
),并将其放入广口瓶中;
④从分液漏斗中缓滴入稀![]() ,至不再产生气体为止;
,至不再产生气体为止;
⑤缓缓鼓入空气数分钟,然后称量干燥管Ⅰ的总质量(设为 ).
).
根据上述实验,回答下列问题:
(1)鼓入空气的目的是___________________________________.
(2)装置A中液体②应为_________,其作用是__________,如撤去装置A,直接向装置B中缓缓鼓入空气,测定结果将_________(填“偏大”、“偏小”或“不变”).
(3)装置C的作用是_____,如果撤去装置C,则会导致实验结果________(填“偏大”、“偏小”或“不变”).
(4)干燥管Ⅱ的作用是____________________________________.
(5)上述实验的操作④和⑤,都要求缓缓进行,其理由是________,如果这两步操作太快,则会导致实验测定结果_______(填“偏大”、“偏小”或“不变”).
(6)根据实验,纯碱中![]() 的质量分数的计算式为__________.
的质量分数的计算式为__________.
工业品纯碱中常含有少量的NaCl等杂质,图中的仪器装置可用来测定纯碱中![]() 的质量分数,图中标号:①空气,②某溶液,③纯碱样品,④稀
的质量分数,图中标号:①空气,②某溶液,③纯碱样品,④稀 ,⑤浓
,⑤浓 ,⑥碱石灰,⑦碱石灰.
,⑥碱石灰,⑦碱石灰.

实验步骤是:
①检查装置的气密性;
②准确称量盛有碱石灰干燥管Ⅰ的质量(设为 );
);
③准确称量一定量的纯碱的质量(设为 ),并将其放入广口瓶中;
),并将其放入广口瓶中;
④从分液漏斗中缓滴入稀![]() ,至不再产生气体为止;
,至不再产生气体为止;
⑤缓缓鼓入空气数分钟,然后称量干燥管Ⅰ的总质量(设为 ).
).
根据上述实验,回答下列问题:
(1)鼓入空气的目的是___________________________________.
(2)装置A中液体②应为_________,其作用是__________,如撤去装置A,直接向装置B中缓缓鼓入空气,测定结果将_________(填“偏大”、“偏小”或“不变”).
(3)装置C的作用是_____,如果撤去装置C,则会导致实验结果________(填“偏大”、“偏小”或“不变”).
(4)干燥管Ⅱ的作用是____________________________________.
(5)上述实验的操作④和⑤,都要求缓缓进行,其理由是________,如果这两步操作太快,则会导致实验测定结果_______(填“偏大”、“偏小”或“不变”).
(6)根据实验,纯碱中![]() 的质量分数的计算式为__________.
的质量分数的计算式为__________.
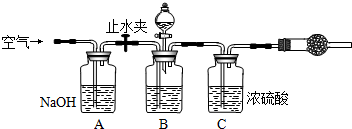
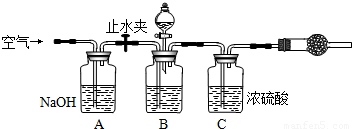
(10分)工业纯碱中常常含有NaCl、Na2SO4等杂质。为测定某工业纯碱的纯度,设计了如下图实验装置。
依据实验设计,请回答:
(1)装置中盛装稀硫酸的仪器名称是 ;
装置D的作用是
。
(2)为达到测定某工业纯碱的纯度实验目的,一次实验中至少应 进行称量操作的次数为 。
(3)若不考虑操作、药品及其用量等方面
的影响,该实验测得结果会 (填“偏高”、“偏低”、“无影响”);
原因是
(你若认为无影响,该空不用回答)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com