
题目列表(包括答案和解析)
| A、药片变色、潮解,则不宜服用 | B、复方氢氧化铝片常用来治疗胃酸过多症 | C、“药是三分毒”,因此,有病不要服药 | D、实行“食盐加碘”是控制碘缺乏症的有效途径之一 |
为了预防碘缺乏症,国家规定每千克食盐中应含40~50mg碘酸钾。碘酸钾晶体有较高的稳定性,但在酸性溶液中,碘酸钾是一种较强的氧化剂,能跟某些还原剂作用生成碘;在碱性溶液中,碘酸钾能被氯气、次氯酸等强氧化剂氧化为更高价的碘的含氧酸盐。
【问题1】工业生产碘酸钾的流程如下:
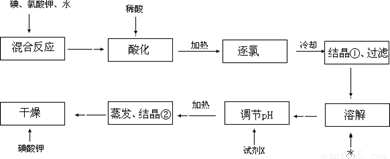
(1)碘、氯酸钾和水混合后的反应为(未配平):I2+KClO3+H2O→KH(IO3)2+KCl+Cl2↑。该方程式配平时,系数有多组,原因是 。
(2)X的化学式为 ;写出用试剂X调节pH的化学方程式: 。
(3)生产中,如果省去“酸化”、“逐氯”、“结晶①、过滤”这三步操作,直接用试剂X调整反应后溶液的pH,对生产碘酸钾有什么具体影响? 。
【问题2】已知:KIO3+5KI+3H2SO4→3K2SO4+3I2+3H2O; I2+2S2O32-→2I-+S4O62-。
(4)检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应。用四氯化碳检验碘单质时,看到的明显现象有 。
(5)测定加碘食盐中碘的含量,学生乙设计的实验步骤如下:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL恰好反应。
则加碘食盐样品中的碘元素含量是 mg/kg(以含w的代数式表示)。
(6)学生丙又对纯净的NaCl(不含KIO3)进行了下列实验:
|
操作步骤 |
实验现象 |
|
取1g纯净的NaCl,加3mL水配成溶液。 |
溶液无变化 |
|
滴入5滴淀粉溶液和1mL 0.1 mol·L-1 KI溶液,振荡。 |
溶液无变化 |
|
然后再滴入1滴1mol·L-1的H2SO4,振荡。 |
溶液变蓝色 |
①推测实验中产生蓝色现象的可能原因,用离子方程式表示 。
②根据学生丙的实验结果,请对学生乙的实验结果作出简要评价: 。
(16分)化学提高了人们生存的质量,生活质量的提高又促进了化学发展。
(1)下列说法错误的是( )
A.药片变色、潮解,则不宜服用
B.复方氢氧化铝片常用来治疗胃酸过多症
C. “药是三分毒”,因此,有病不要服药
D.实行“食盐加碘”是控制碘缺乏症的有效途径之一
(2)下列做法中错误的是( )
A.鱼、肉、虾等食品用福尔马林防腐保鲜
B.国际奥委会禁止使用的兴奋剂——麻黄碱
C.向伤口处涂一定浓度的双氧水溶液可以杀菌消毒
D.误食铜、汞、铜等重金属,立即喝牛奶或鸡蛋清解毒
(3)肉类如果长时间接触空气,其红色就会被氧化成难看的棕色,如果加入亚硝酸钠,就可以使肉保持鲜红,这是利用了亚硝酸钠的什么性质( )
A.氧化性 B.还原性 C.防腐 D.着色
(4)环境污染已成为人类社会面临的重大威胁,各种污染数不胜数,下列各项中与环境污染无关的是( )
①温室效应 ②赤潮 ③酸雨 ④臭氧空洞
⑤水俣病 ⑥大脖子病 ⑦水华 ⑧潮汐
A.①② B.③④ C.⑤⑥ D.⑥⑧
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com