
题目列表(包括答案和解析)
已知热化学方程式:
Mg(OH)2(s)=MgO(s)+H2O(g); △H1=+81.5kJ·mol-1
Al(OH)3(s)=![]() Al2O3(s)+
Al2O3(s)+![]() H2O(g); △H2=+87.7kJ·mol-1
H2O(g); △H2=+87.7kJ·mol-1
其中,氧化镁熔点2852℃;氧化铝熔点2050℃
(1)Mg(OH)2和Al(OH)3起阻燃作用的主要原因是
(2)等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是
原因是
(3)常用阻燃剂主要有三类:A.卤系,如四溴乙烷(熔点0℃,沸点:243.5℃);B.磷系,如磷酸三苯酯(熔点48.5℃,沸点370℃);C.无机类,主要是Mg(OH)2和Al(OH)3。从环保的角度考虑,应用时较理想的阻燃剂是 (填代号),理由是
已知热化学方程式:
Mg(OH)2(s)=MgO(s)+H2O(g); △H1=+81.5kJ·mol-1
Al(OH)3(s)=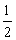 Al2O3(s)+
Al2O3(s)+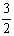 H2O(g);
△H2=+87.7kJ·mol-1
H2O(g);
△H2=+87.7kJ·mol-1
其中,氧化镁熔点2852℃;氧化铝熔点2050℃
(1)Mg(OH)2和Al(OH)3起阻燃作用的主要原因是
(2)等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是
原因是
(3)常用阻燃剂主要有三类:A.卤系,如四溴乙烷(熔点0℃,沸点:243.5℃);B.磷系,如磷酸三苯酯(熔点48.5℃,沸点370℃);C.无机类,主要是Mg(OH)2和Al(OH)3。从环保的角度考虑,应用时较理想的阻燃剂是 (填代号),理由是
(9分)氢氧化镁用于制药工业,还是重要的绿色阻燃剂。
I、治疗胃酸过多药物Stmoache的有效成分为Mg(OH)2。
(1)该药物治疗胃酸(主要成分为盐酸)过多症时反应的离子方程式:____________________________________________。
Ⅱ、已知:Mg (s)+2H2O(g)=Mg(OH)2(s)+H2(g) △H1=-441kJ·mol-1
H2O(g)=H2(g)+![]() O2(g) △H2=+242kJ·mol-1
O2(g) △H2=+242kJ·mol-1
Mg(s)+![]() O2(g)=MgO(s) △H3=-602kJ·mol-1
O2(g)=MgO(s) △H3=-602kJ·mol-1
(2)氢氧化镁分解的热化学方程式是_______________________________________。
(3)氢氧化镁可以作为阻燃剂的原因____________________。(写一条即可)
Ⅲ、某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯
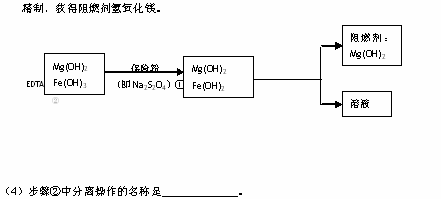
(5)步骤①中的反应如下:6Fe(OH)3 +S2O42-+2OH- =6Fe(OH)2 +2SO42-+4H2O。
每消耗0.1mol保险粉(Na2S2O4)时,转移电子的数目是 NA。
(6)已知EDTA只能与溶液中的Fe2+反应生成易溶于水的物质,不与Mg(0H)2反应。虽然Fe(OH)2难溶于水,但步骤②中随着EDTA的加入,最终能够将Fe(OH)2除去并获得纯度高的Mg(OH)2。请从沉淀溶解平衡的角度加以解释。
答:___________________________________________________________________。
(9分)氢氧化镁用于制药工业,还是重要的绿色阻燃剂。
I、治疗胃酸过多药物Stmoache的有效成分为Mg(OH)2。
(1)该药物治疗胃酸(主要成分为盐酸)过多症时反应的离子方程式:____________________________________________。
Ⅱ、已知:Mg (s)+2H2O(g)=Mg(OH)2(s)+H2(g) △H1=-441kJ·mol-1
H2O(g)=H2(g)+![]() O2(g) △H2=+242kJ·mol-1
O2(g) △H2=+242kJ·mol-1
Mg(s)+![]() O2(g)=MgO(s) △H3=-602kJ·mol-1
O2(g)=MgO(s) △H3=-602kJ·mol-1
(2)氢氧化镁分解的热化学方程式是_______________________________________。
(3)氢氧化镁可以作为阻燃剂的原因____________________。(写一条即可)
Ⅲ、某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制,获得阻燃剂氢氧化镁。
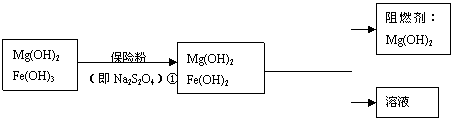

(4)步骤②中分离操作的名称是_____________。
(5)步骤①中的反应如下:6Fe(OH)3 +S2O42-+2OH- =6Fe(OH)2 +2SO42-+4H2O。
每消耗0.1mol保险粉(Na2S2O4)时,转移电子的数目是 NA。
(6)已知EDTA只能与溶液中的Fe2+反应生成易溶于水的物质,不与Mg(0H)2反应。虽然Fe(OH)2难溶于水,但步骤②中随着EDTA的加入,最终能够将Fe(OH)2除去并获得纯度高的Mg(OH)2。请从沉淀溶解平衡的角度加以解释。
答:___________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com