
题目列表(包括答案和解析)
|
已知:H+在溶液中以水合氢离子的形式存在:H++H2O ①2Na+2NH3 ②CaO+2NH4Cl ③3Mg(NH2)2 ④NH4Cl+NaNH2 | |
A. |
③ |
B. |
② |
C. |
②③ |
D. |
①②③④ |
| |||||||||||||||||||||||||||||||||
某矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如下:
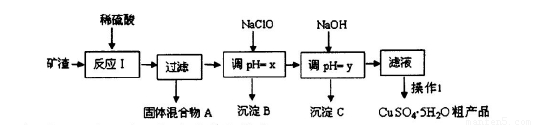
已知: ①Cu2O +2 H+=Cu + Cu2++H2O
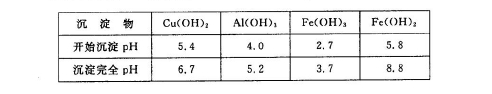
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
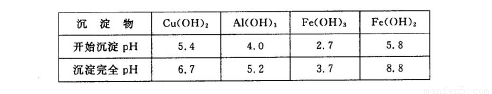
请回答下列问题:
(1)为了加快反应I的速率,可以采取的措施是??????????????????????????? (写2点)。
(2)固体混合物A中的成分是????????????????????????????? 。
(3)反应I完成后,铁元素的存在形式为??? (填离子符号);写出生成该离子的离子方程式?????????? 。
(4)操作1主要包括:?????????? 、???????????? 、??????? 。洗涤CuSO4?5H2O粗产品不能用大量水洗,而用冰水洗涤。原因是????????????????????????????????????????? 。
(5)用惰性电极电解胆矾溶液一段时间,加人0.1 mol的Cu(OH)2可恢复溶液原况(浓度、成分),则电解时转移电子的物质的量为???????????????????????????? .。
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为 ????????? 。
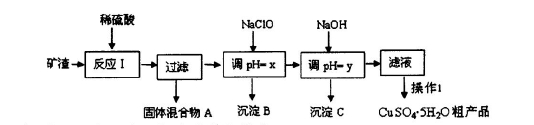
某矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如下:
已知: ①Cu2O +2 H+="Cu" + Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表: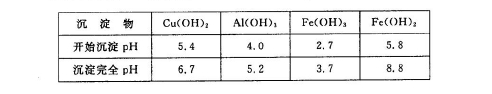
请回答下列问题:
(1)为了加快反应I的速率,可以采取的措施是 (写2点)。
(2)固体混合物A中的成分是 。
(3)反应I完成后,铁元素的存在形式为 (填离子符号);写出生成该离子的离子方程式 。
(4)操作1主要包括: 、 、 。洗涤CuSO4?5H2O粗产品不能用大量水洗,而用冰水洗涤。原因是 。
(5)用惰性电极电解胆矾溶液一段时间,加人0.1 mol的Cu(OH)2可恢复溶液原况(浓度、成分),则电解时转移电子的物质的量为 .。
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com