
题目列表(包括答案和解析)
常见的短周期元素A、B、C、D、E的原字序数穰沃增夫。常温下,A、C可形成A2C2和A2C两种液态化合物,B原子最外层电子数是次外层电子数的2倍,D原子电子层数与最外层电予数相等,E与C同主族。
(1)上述五种元素中,非金属性最强的是 (填写元素名称)。
(2)元素D形成的简单离子的原子结构示意图为 。
(3)A的单质与C的单质在强酸性条件下构成燃料电池,其正极反应式为 。
(4)上述五种元素,由其中三种元素组成的易溶于水的物质中,能促进水电离的物质是:
(写出一种物质的化学式,下同),能抑制水电离的物质是: 。
(5)常温常压时,2.8gBC气体在3.2gC2气体中完全燃烧,生成BC2气体时放出28.3kJ的热量,则表示BC燃烧的热化学方程式为 。
常见的短周期元素A、B、C、D、E的原字序数穰沃增夫。常温下,A、C可形成A2C2和A2C两种液态化合物,B原子最外层电子数是次外层电子数的2倍,D原子电子层数与最外层电予数相等,E与C同主族。
(1)上述五种元素中,非金属性最强的是 (填写元素名称)。
(2)元素D形成的简单离子的原子结构示意图为 。
(3)A的单质与C的单质在强酸性条件下构成燃料电池,其正极反应式为 。
(4)上述五种元素,由其中三种元素组成的易溶于水的物质中,能促进水电离的物质是:
(写出一种物质的化学式,下同),能抑制水电离的物质是: 。
(5)常温常压时,2.8gBC气体在3.2gC2气体中完全燃烧,生成BC2气体时放出28.3kJ的热量,则表示BC燃烧的热化学方程式为 。
常见的短周期元素A、B、C、D、E的原子序数依次增大。常温下,A、C可形成A2C2和A2C两种液态化合物,B原子最外层电子数是次外层电子数的2倍,D原子电子层数与最外层电子数相等,E与C同主族![]()
(1)写出B、D两元素的元素符号;B. D. 。
(2)上述五种元素中,非金属性最强的是 (填写元素名称),最高价氧化物对应水化物酸性最强的是 (写化学式)。
(3)元素D形成的简单离子的结构示意图为 。D的单质与第三周期A的同主族元素最高价氧化物对应水化物反应的离子方程式为 。
(4)B的单质与E的最高价氧化物对应水化物浓溶液共热反应的化学方程式为: 。
 短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子.A、C位于同一主族,A为非金属元素,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等.E单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏.
短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子.A、C位于同一主族,A为非金属元素,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等.E单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏.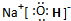
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com