
题目列表(包括答案和解析)
 ”结构的有机物不能稳定存在.请结合①②有关信息,分析如下转化关系,图中所用NaOH都是足量的,回答问题:
”结构的有机物不能稳定存在.请结合①②有关信息,分析如下转化关系,图中所用NaOH都是足量的,回答问题:





 做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是
做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是 ).在空气中微量水催化下发生加聚反应,迅速固化而将物粘牢.请写出“502胶”发生粘合作用的化学方程式:
).在空气中微量水催化下发生加聚反应,迅速固化而将物粘牢.请写出“502胶”发生粘合作用的化学方程式:

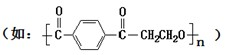
 )也是一种粘合剂,在空气中稳定,但在隔绝空气(缺氧)时,分子中双键断开发生聚合而固化.工业上用丙烯酸和某种物质在一定条件下反应可制得这种粘合剂.这一制取过程的化学方程式为
)也是一种粘合剂,在空气中稳定,但在隔绝空气(缺氧)时,分子中双键断开发生聚合而固化.工业上用丙烯酸和某种物质在一定条件下反应可制得这种粘合剂.这一制取过程的化学方程式为 +HOCH2CH2OH
+HOCH2CH2OH| 浓硫酸 |
| △ |
 +2H2O
+2H2O +HOCH2CH2OH
+HOCH2CH2OH| 浓硫酸 |
| △ |
 +2H2O
+2H2O .已知含有
.已知含有 结构的物质不能稳定存在.请另外任写四种含-CH=CH-结构的链状同分异构体的结构简式:
结构的物质不能稳定存在.请另外任写四种含-CH=CH-结构的链状同分异构体的结构简式:| 一定条件 |
 可用做普通胶水,它的羟基可全部与正丁醛缩合脱水,得到含六原子环的强力粘合剂聚乙烯缩丁醛.请写出制取聚乙烯缩丁醛的化学方程式:
可用做普通胶水,它的羟基可全部与正丁醛缩合脱水,得到含六原子环的强力粘合剂聚乙烯缩丁醛.请写出制取聚乙烯缩丁醛的化学方程式:


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com