实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如下方案:
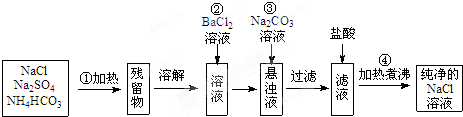
如果此方案正确,那么:
(1)操作①中碳酸氢铵受热(100℃以上)可分解生成氨气、水和二氧化碳的混合气,该混合气的平均摩尔质量为
26.3g/mol
26.3g/mol
.(数值保留到小数点后一位)
(2)操作②为什么不能改为加硝酸钡溶液?
改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,以后操作中无法除去
改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,以后操作中无法除去
.
(3)操作③的目的是
发生反应Na2CO3+BaCl2═BaCO3↓+2NaCl,除去过量的Ba2+
发生反应Na2CO3+BaCl2═BaCO3↓+2NaCl,除去过量的Ba2+
(结合化学方程式回答).
(4)操作④的目的是
除去滤液中溶解的CO2和多余的盐酸
除去滤液中溶解的CO2和多余的盐酸
.





