
题目列表(包括答案和解析)
类比是化学学习中常用的方法之一,已知硝酸能把铁氧化成 Fe ( NO3)3,但当铁过量时,产物是 Fe (NO3) 2 。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当 C12 足量时生成 FeC13 , 当铁粉过量时产物是 FeCl2 。为验证该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的 C12 中点燃,取其表面生成物并分别编号为 A、B ,然后通过实验确定其成分。
探究过程如下:
提出假设: A 是 FeCl3 , B 是 FeCl2 。
(1) 设计实验方案:分别取 A、B 的溶液均进行以下实验,但实验现象相同。请填写下表中的相应空格。
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 | ____________________ | 固体物质中有FeCl3 |
| 分别向KMnO4溶液中加适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含_______ |
(2)根据上述实验结论,写出C12与铁粉加热时发生反应的化学方程式:
____________________________________________________________。
(3)为进一步探究 FeC13 溶液的性质,他又利用 A 溶液做了如下一些实验,其中明显错误的是_______________(填写序号)。
A.将 A 溶液滴入淀粉碘化钾溶液中,可得到蓝色液体,该液体能产生丁达尔现象
B.向 A 溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在 A 溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将 A 溶液加热蒸干并灼烧,得到FeC13固体
(4)FeCl3溶液常作印刷电路铜板腐蚀剂,腐蚀后的废液中含有 FeC13、FeCl2、CuCl2,
某研究性学习小组的同学们设计了两种从废液中回收 Cu的方案:
方案1:向废液中加入过量的铁粉,充分反应后,过滤。在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得到铜。
该方案中涉及的四种阳离子的氧化性由强到弱的顺序为:
方案2 :在废液中加入适量的盐酸调节溶液的 pH = 1 ,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的 Cu 已全部析出。该方案中铜作_________极,该电极上所发生的电极反应为(若有多个电极反应,请按照反应发生的先后顺序全部写出)______________________________________________________________。
方案2 在电极上直接回收铜,操作上比方案 1 简便,但方案 2 也有不足之处,主要表现为:____________________________________
某同学探究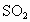 与
与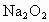 的反应原理,请你帮助他完成下列内容:
的反应原理,请你帮助他完成下列内容:
(1)写出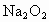 与
与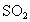 反应的化学方程式:____________________________________________________________。
反应的化学方程式:____________________________________________________________。
(2)该同学为检验反应中是否有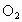 生成,拟用如图所示装置进行实验,装置B的作用是_________,D的作用是________________________。
生成,拟用如图所示装置进行实验,装置B的作用是_________,D的作用是________________________。
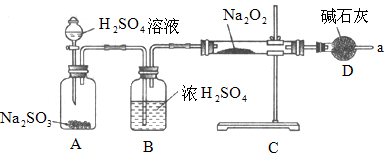
(3)为确定反应产物,该同学设计了以下实验步骤,你认为应进行的操作且按正确顺序排列的是_________(填序号)。
A.带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧
B.将C装置中反应后的固体物质溶于适量水配成溶液
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成
(2)某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗?___________。简要说明理由_________________________________________________________________。
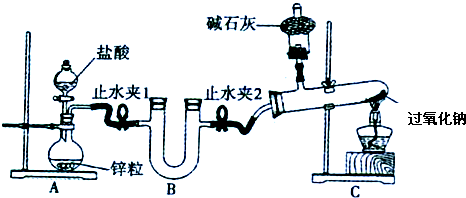
(3)该同学无法断定SO2和Na2O2反应中是否有氧气生成,拟用下列装置进行实验。
(已知:Na2SO3+2H2SO4![]() Na2SO4+H2O+SO2↑)
Na2SO4+H2O+SO2↑)
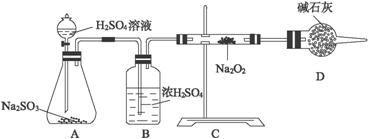
装置B的作用是__________________________________________________________。
D的作用是____________________________________________________________。
(4)为确认SO2和Na2O2的反应产物,该同学设计了以下实验步骤,请你从中挑选出正确的选项并按操作顺序排列(填序号)_______________。
A.用带火星的木条靠近干燥管口,观察木条是否复燃
B.用C装置中反应后的固体物质溶于适量水配成溶液
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成
在75℃左右,用HgSO4作催化剂,乙炔可水化为乙醛.但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种.现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末五种物质制乙醛,装置如图: 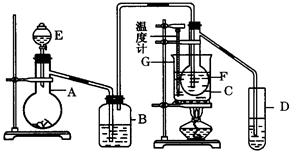
请回答以下问题:
(1) 实验开始时,仪器A中盛放电石,B中应装入 ,其作用是 .
(2) 仪器D中盛放水,其作用是 .
(3) 蒸馏烧瓶F中应加入HgO和另外两种试剂,若将三者分别直接加入,请按加入的先
后顺序写出包括HgO在内的各试剂名称 ,将HgO加入F中的操作方法是 .
(4) 装置图中,加热F的方式叫 ,所选用温度计G的量程表示正确的是__________(填代号).
| A.0℃~50℃ | B.0℃~100℃ | C.0℃~200℃ | D.0℃~360℃ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com