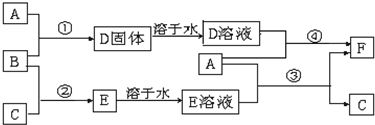
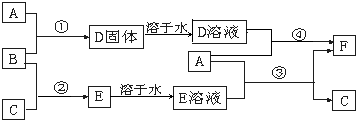
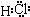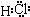C、D、G、I均为短周期元素形成的单质,D、G、I为常见非金属气态单质.D的最外层电子数是次外层电子数的3倍,C、G同周期,且最外层电子数相差4,它们的简单离子电子层结构不同.相互间有如下转化关系:
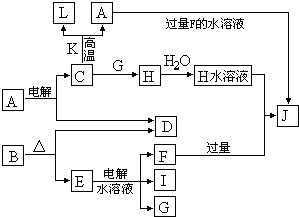
请填空:
(1)D与I能形成原子个数比为1:1的共价化合物,请写出其分子式:
H2O2
H2O2
;
G与I也能形成原子个数比为1:1的共价化合物,请写出其电子式:
.
(2)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,写出电解1L1mol?L
-1的E水溶液的化学方程式:
,当溶液的pH=13时,理论上生成G的单质在标准状况下的体积为
1.12L
1.12L
;若将上述两电极材料调换,则阳极上的电极反应为
Fe-2e-=Fe2+
Fe-2e-=Fe2+
.
(3)化合物K 中含有组成单质L的元素,且该元素的质量分数为70%.反应C→L的化学方程式是
(4)写出A+F→J的离子方程式:
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.



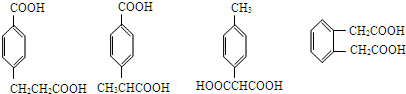 任意一种
任意一种 任意一种
任意一种