
题目列表(包括答案和解析)
| |||||||||||||||||||||||||||||
(16分)下列物质:①水晶 ②干冰 ③氨气 ④白磷 ⑤氩 ⑥氯化钠
⑦铁 ⑧晶体硅 ⑨过氧化钠 ⑩![]() 。其中:
。其中:
(1) 晶体⑥中1个阳离子周围有 个阴离子,它们围成的几何体为 。
(2)熔化时只破坏共价键的晶体是 (填结构式)
(3) ⑥⑦⑧三种晶体一定条件下能导电,导电时发生化学变化的是 。(填序号)
(4) 含有极性键的非极性分子是 (填序号),用电子式表示其形成过程 。
(5) 将 ①②④⑥⑧⑩按照熔沸点由高到低的顺序排列 (填序号),
(6)1 mol金刚石、水晶和白磷中含有共价键的数目之比为
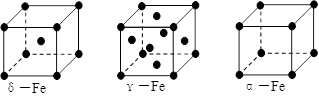
(7)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为 。
(16分)下列物质:①水晶 ②干冰 ③氨气 ④白磷 ⑤氩 ⑥氯化钠
⑦铁 ⑧晶体硅 ⑨过氧化钠 ⑩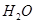 。 其中:
。 其中:
(1) 晶体⑥中1个阳离子周围有 个阴离子,它们围成的几何体为 。
(2)熔化时只破坏共价键的晶体是 (填结构式)
(3) ⑥⑦⑧三种晶体一定条件下能导电,导电时发生化学变化的是 。(填序号)
(4) 含有极性键的非极性分子是 (填序号),用电子式表示其形成过程 。
(5) 将 ①②④⑥⑧⑩按照熔沸点由高到低的顺序排列 (填序号),
(6)1 mol金刚石、水晶和白磷中含有共价键的数目之比为
(7)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为 。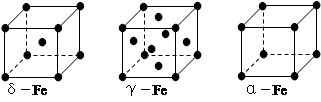
(16分)下列物质:①水晶 ②干冰 ③氨气 ④白磷 ⑤氩 ⑥氯化钠
⑦铁 ⑧晶体硅 ⑨过氧化钠 ⑩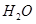 。
其中:
。
其中:
(1) 晶体⑥中1个阳离子周围有 个阴离子,它们围成的几何体为 。
(2)熔化时只破坏共价键的晶体是 (填结构式)
(3) ⑥⑦⑧三种晶体一定条件下能导电,导电时发生化学变化的是 。(填序号)
(4) 含有极性键的非极性分子是 (填序号),用电子式表示其形成过程 。
(5) 将 ①②④⑥⑧⑩按照熔沸点由高到低的顺序排列 (填序号),
(6)1 mol金刚石、水晶和白磷中含有共价键的数目之比为
(7)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为 。
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com