
题目列表(包括答案和解析)
X、Y、Q、R是同一短周期的元素。已知:
(1)X的最高正价绝对值是最低负价绝对值的3倍,其气态氢化物与最高价氧化物的相对分子质量之比是1∶2.35。
(2)Y和Q的气态氢化物分子组成分别是YH4和QH3。R的氢化物化学式为RH2,但常温时不是气态的。
(3)另有一种元素E,其阳离子和X的阴离子带有等量的相反电荷,且核外电子数相同。请指出X、Y、Q、R、E各是什么元素以及它们在元素周期表中的位置。
(1)X的最高正价绝对值是最低负价绝对值的3倍,其气态氢化物与最高价氧化物的相对分子质量之比是1∶2.35。
(2)Y和Q的气态氢化物分子组成分别是YH4和QH3。R的氢化物化学式为RH2,但常温时不是气态的。
(3)另有一种元素E,其阳离子和X的阴离子带有等量的相反电荷,且核外电子数相同。请指出X、Y、Q、R、E各是什么元素以及它们在元素周期表中的位置。
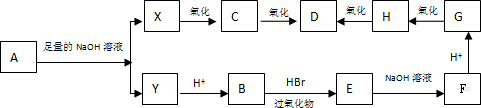
X、Y、Z、D、E、F是原子序数依次增大的六种常见元素。E的单质在Z2中燃烧的产物可使品红溶液褪色。F和Z元素形成的化合物F3Z4具有磁性。X的单质在Z2中燃烧可生成XZ和XZ2两种气体。D的单质是一种金属,该金属在XZ2中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)F元素在周期表中的位置是____________,Y的单质分子的结构式为______________,DZ的电子式为____________。
(2)X元素形成的同素异形体的晶体类型可能是(填序号)__________。
① 原子晶体 ② 离子晶体 ③金属晶体 ④分子晶体
(3)X、Y、Z形成的10电子氢化物中,X、Y的氢化物沸点较低的是(写化学式):____________;Y、Z的氢化物分子结合H+能力较强的是(写化学式)______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com