
题目列表(包括答案和解析)

请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式____________________________。
(2)完成该实验所需的装置是(填标号)_______________。
(3)所选用的装置的连接顺序是_______________(填各接口的字母,连接用的胶管可以省略)。
现有一定量的含Na2O杂质的Na2O2试样,请从下图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体、20%盐酸和蒸馏水).(已知此状况下O2、CO2的密度分别为1.429 g·L-1,1.977 g·L-1)
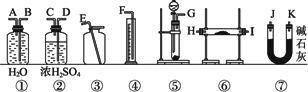
请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式________.
(2)完成该实验所需的装置是(填标号)________.
(3)所选用的装置的连接顺序是________(填各接口的字母,连接用的胶管可以省略).
现有一定量含
Na2O杂质的Na2O2试样,利用下图所示的实验装置可以测定其纯度.(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)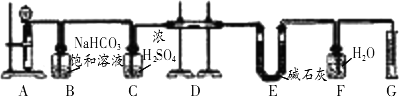
(1)实验前必须检查装置的气密性.仪器连接好后,在________中加适量的水,关闭装置A中分液漏斗的活塞后微热试管,若看到________,说明装置气密性好.
(2)装置A中的液体试剂应选用盐酸而不选用硫酸,理由是________.
(3)装置B的作用是________,装置C的作用是________,装置E中碱石灰的作用是________.
(4)装置D中发生反应的化学方程式为________.
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体的体积为224 mL(标准状况下),则Na2O2试样的纯度为________.
| 读数次数 | 质量/g | |
| 第1次 | 196.30 | |
| 第2次 | 196.15 | |
| 锥形瓶十水十试样 | 第3次 | 196.05 |
| 第4次 | 196.00 | |
| 第5次 | 196.00 |


| 读数次数 | 质量/g | |
锥形瓶十水十试样 |
第1次 | 196.4 |
| 第2次 | 196.2 | |
| 第3次 | 196.1 | |
| 第4次 | 196.0 | |
| 第5次 | 196.0 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com