
题目列表(包括答案和解析)
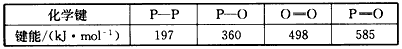

白磷(P4)是正四面体构型的分子,当与氧气作用形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键再结合一个氧原子.化学反应可视为旧键断裂和新键形成的过程.现提供以下化学键的键能(kJ/mol).P-P键:198 kJ/mol;P-O键:360 kJ/mol;O=O键:498 kJ/mol;P=O键:585 kJ/mol.试根据这些数据,计算出以下反应的反应热:P4(S,白磷)+5O2(g)=P4O10(s);△H=________.
(2分)白磷(P4)是正四面体构型的分子,当与氧气作用形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键再结合一个氧原子。化学反应可视为旧键断裂和新键形成的过程。现提供以下化学键的键能(kJ/mol)。P-P键:198 kJ /mol ;P-O键:360 kJ /mol ;O=O键:498 kJ /mol ;P=O键:585 kJ /mol。试根据这些数据,计算出以下反应的反应热:P4(S,白磷)+ 5O2(g)= P4O10(s);
ΔH= 。
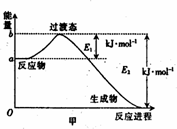
(1)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成,而是在反应物到生成物的过程中经过一个高能量的过渡态.图甲是白磷(P4)和O2反应生成P4O10过程中能量变化示意图,请写出白磷(P4)和O2反应生成P4O10的热化学方程式:________(△H用含E1和E2的代数式表示,其中E1、E2均大于0).
(2)白磷(图乙)是正四面体构型的分子,当与氧气作用形成P4O6时,相当于每两个磷原子之间插入一个氧原子(如图丙).当形成P4O10时,相当于在P4O6的分子中每个磷原子又以双键结合一个氧原子(如图丁).

请在图丙的示意图中把磷原子用钢笔或铅笔把磷原子涂黑.
(3)进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1mol化学键时所需吸收的能量.下表是部分化学键的键能数据:
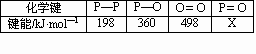
已知白磷(P4)的燃烧热为2982kJ·mol—1,白磷完全燃烧的产物结构如图丁所示,则上表中x=________
(4)写出1molP4与O2反应生成固态P4O6的反应热△H=________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com