
题目列表(包括答案和解析)
据此判断其正极是__________,负极是__________,电解质溶液是__________,正极反应是__________,负极反应是__________。当转移0.5 Na个电子,蓄电池内消耗H2SO4的物质的量为__________。
电极反应: 负极:Pb+![]() -2e-
-2e-![]() PbSO4
PbSO4
正极:PbO2+![]() +4H++2e-
+4H++2e-![]() PbSO4+2H2O
PbSO4+2H2O
总反应式:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O
2PbSO4+2H2O
下列对铅蓄电池的叙述正确的是( )
A.充电时化学能转化成电能
B.充电时电能转化为化学能
C.在充、放电过程中只有化学能与电能间的转化
D.在充、放电过程中也有其他形式能的转化,如电能转化为热能
Pb+PbO2+4H++2![]()
![]() 2PbSO4+2H2O,现有装置如下图,则下列说法正确的是
2PbSO4+2H2O,现有装置如下图,则下列说法正确的是
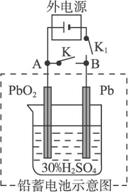
A.放电时负极反应是Pb-2e-====Pb2+,充电时阴极反应是PbSO4+2H2O-2e-====PbO2+4H+ +![]()
B.闭合K断开K1,电流的方向是从B到A
C.放电过程中,溶液的pH不断减小
D.放电时,线路上若有1 mol电子通过,则消耗硫酸也是1 mol
(1)铅蓄电池在放电时的负极反应为_________.
其在充电时的阳极反应为_________.
(2)镍镉碱性充电电池在充电时的总反应的化学方程式为_________.
(3)上述两种电池使用一段时间后,一个内阻明显增大,另一个内阻却几乎不变的主要原因可能是_________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com