某市工商局查获400克袋装中老年补钙营养奶粉1 401包.这种奶粉被鉴定为所含亚硝酸盐残留量高出正常值7.8倍,长期食用可能致癌.已知NaNO
2能发生如下反应:2NaNO
2+4HI═2NO+I
2+2NaI+2H
2O.
(1)上述反应中氧化剂是
NaNO2
NaNO2
,若有0.75mol的还原剂被氧化,则被还原的氧化剂有
0.75
0.75
mol.
(2)根据上述反应,可以用试纸和生活中常见的物质进行实验,以鉴别NaNO
2和NaCl,可选用的物质有①自来水;②淀粉碘化钾试纸;③淀粉;④白糖;⑤食醋;⑥白酒.进行实验时,必须选用的物质有
②⑤
②⑤
.
(3)某厂废切削液中,含2%~5%的NaNO
2,直接排放会造成污染,下列试剂中
②
②
(填序号)能使NaNO
2转化为不引起二次污染的N
2,反应的化学方程式为
NaNO2+NH4Cl═NaCl+N2↑+2H2O
NaNO2+NH4Cl═NaCl+N2↑+2H2O
.
①NaCl ②NH
4Cl ③H
2O
2 ④浓H
2SO
4.

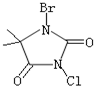 (2010?江苏一模)开发具有广谱、高效、低毒的杀菌、消毒剂是今后发展的趋势.
(2010?江苏一模)开发具有广谱、高效、低毒的杀菌、消毒剂是今后发展的趋势.