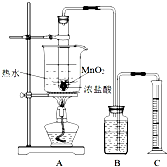
实验室常用浓盐酸与二氧化锰反应制取氯气.浓盐酸和二氧化锰反应过程中,浓盐酸的浓度不断降低,当盐酸浓度降至临界浓度时,反应停止.
方法一:
甲同学利用图装置,测定盐酸浓度降至临界浓度时 反应生成氯气的体积,来探究在某温度下浓盐酸与二氧化锰反应的临界浓度.
方法:A中试管有足量的MnO
2,往其中加入10mol/L的浓盐酸,控制温度为80℃进行反应.甲同学进行了三次同样的实验,收集气体(体积均换算成标准状况),数据如下表:
|
第一次实验 |
第二次实验 |
第三次实验 |
| 盐酸的用量 |
10.0mL |
10.0mL |
10.0mL |
| 氯气的体积 |
225mL |
192mL |
223mL |
回答下列问题:
(1)请写出A中试管内反应的离子方程式
.
(2)检验该装置的气密性的方法是
.
(3)B中加入的溶液为
.
(4)为计算与二氧化锰反应的浓盐酸临界浓度,甲同学的第
次实验数据应舍去.经计算反应的盐酸临界浓度为
.
方法二:
(5)乙同学认为该实验有不足之处:浓盐酸易挥发,会造成上述所测的临界浓度
(填“偏高”“偏低”).
乙同学提出可直接用反应后A中的溶液来测定盐酸的临界浓度:
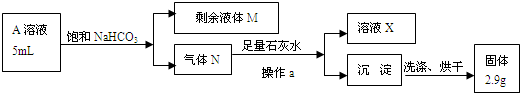
(6)以上图表中操作a的名称是
.
(7)请写出A溶液中的物质与NaHCO3溶液反应的离子方程式:
.
(8)根据以上数据,浓盐酸与二氧化锰制氯气的反应中浓盐酸的临界浓度为
.

 实验室常用浓盐酸与二氧化锰反应制取氯气.浓盐酸和二氧化锰反应过程中,浓盐酸的浓度不断降低,当盐酸浓度降至临界浓度时,反应停止.
实验室常用浓盐酸与二氧化锰反应制取氯气.浓盐酸和二氧化锰反应过程中,浓盐酸的浓度不断降低,当盐酸浓度降至临界浓度时,反应停止.