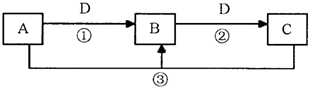
A、B、C三种非金属元素的质子数之和为16,它们的单质在一定条件下两两化合可以生成三种常见的化合物D、E、F.D、F的一个分子中只含有10个电子,常温下D是一种液体,E是一种无色的气体.
(1)B的元素名称是
氢
氢
,C单质的电子式是
:N??N:
:N??N:
.
(2)A、B两元素还能形成一种比D相对分质量大16的化合物,请写出该化合物的一种用途
杀菌消毒
杀菌消毒
;A、C两元素也还能形成一种比E相对分子大16的化合物,请写出实验室制备该化合物反应的化学方程式
Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
.
(3)E、F在一定条件下可以发生反应生成C元素的单质和D,该反应中氧化产物与还原产物的物质的量之比为
2:3
2:3
.
(4)A、B、C三种元素能组成一种原子个数比为3:4:2的常见离子化合物,0.1mol?L
-1的该化合物的水溶液中,溶液显
酸
酸
性(填“酸”、“碱”、“中”),用离子方程式解释原因
NH4++H2O?NH3.H2O+H+
NH4++H2O?NH3.H2O+H+
,该溶液中离子浓度由大到小的顺序是
c(NO3-)>c(NH4+)>c(H+)>c(OH-)
c(NO3-)>c(NH4+)>c(H+)>c(OH-)
.

 Ⅰ
Ⅰ A、B、C三种非金属元素的质子数之和为16,它们的单质在一定条件下两两化合可以生成三种常见的化合物D、E、F.D、F的一个分子中只含有10个电子,常温下D是一种液体,E是一种无色的气体.
A、B、C三种非金属元素的质子数之和为16,它们的单质在一定条件下两两化合可以生成三种常见的化合物D、E、F.D、F的一个分子中只含有10个电子,常温下D是一种液体,E是一种无色的气体.