
题目列表(包括答案和解析)
(14分)
Ⅰ.有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入2 mol/L H2SO4溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如图:

(1)写出甲池中正极的电极反应式: ;
(2)写出乙池中负极的电极反应式: ;
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出 活动性更强(填元素符号)。
(4)由此实验,可得到如下哪些正确结论?( )
A.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动顺序表已过时,已设有实用价值
D.该实验说明化学研究对象复杂、化学反应受条件影响较大,因此应具体问题具体分析
Ⅱ.向一个容积为2 L的密闭容器中充入2 mol A和1
mol B,发生如下反应:2 A(g)
+ B(g)  xC(g) + D(g),反应达到平衡时C的浓度为1.2 mol/L,B的浓度为0.1 mol/L。
xC(g) + D(g),反应达到平衡时C的浓度为1.2 mol/L,B的浓度为0.1 mol/L。
(1)x= ;
(2)若使容器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为
(填“吸热”或“放热”)反应;
(3)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2 mol/L的是 (用序号填空)
①4 mol A + 2 mol B
②3 mol C + 1 mol D
③3 mol C + 1 mol D +1 mol B
 生物质资源是一种污染小的可再生能源.生物质的主要转化途径及主要产物如图.
生物质资源是一种污染小的可再生能源.生物质的主要转化途径及主要产物如图.| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | α 1 | α 2 | α 3 |

X、Y、Z、R 四种短周期元素,原子序数依次增大。已知:X、R处于同一主族,Y元素的最高正价和最低负价的绝对值相等,X与Y元素形成的一种物质是天然气的主要成分;Y与Z元素形成的一种气体会使大气产生“温室效应”。
请回答下列问题:
(1)X、Y、Z三元素所形成的单质或化合物之间,可按下图装置组成燃料电池。
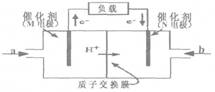
若b口通入的是气体Z2,则a口通入的物质可以是 、 、 (分别填写只由一种、两种、三种元素组成的物质,用化学式表示);M电极的名称为 (填“正极”、“负极”或“阴极”、“阳极”);N电极的电极反应式为 (用化学式表示)。
(2)日常生活中我们经常用到的一种物质其主要成分的化学式为Y18X35Z2R,这种物质的学名为 ,制造这种物质的反应叫 ,写出该反应的化学方程式 。
(3)合成氨工业中,原料气制备的其中一个反应为:YZ+X2Z(g)![]() YZ2+X2;
YZ2+X2;
已知该反应化学平衡常数K和温度T的关系如下表:
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
则下列有关的叙述正确的是 。
A.该反应![]() <0
<0
B.若绝热时(容器内外没有热量交换),改变某一条件平衡向逆反应方向移动,刚容器内气体的温度一定升高
C.若反应在830℃的温度达到平衡状态,反应容器内的四种物质的浓度则一定相等
D.该反应在某温度下,YZ、X2Z的物质的量浓度与时间的关系如下图所示,据此可计算得YZ的转化率为80%

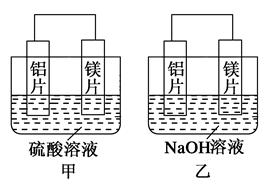
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
(1)写出甲中正极的电极反应式_____________________________。
(2)乙中负极为________,总反应的离子方程式:
______________________________________________________。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出________活动性更强,而乙会判断出________活动性更强。(填写元素符号)
(4)由此实验得出的下列结论中,正确的有________。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析 |
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com