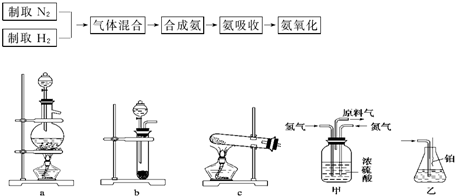
(2009?江门一模)实验室模拟合成氨和氨催化氧化的流程如下:

(l)已知实验室可用饱和亚硝酸钠(NaNO
2)溶液与饱和氯化钱溶液经加热后反应制取氮气,写出该反应的化学方程式:
.
(2)图中,氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有
干燥气体,观察气泡速度,控制氢气和氮气的流速
干燥气体,观察气泡速度,控制氢气和氮气的流速
.
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨
不会
不会
(“会”或“不会”)发生倒吸,原因是
混合气体中含有大量难溶于水的氮气和氢气
混合气体中含有大量难溶于水的氮气和氢气
.
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是
氨的氧化反应是一个放热反应,放出的热使铂丝保持红热
氨的氧化反应是一个放热反应,放出的热使铂丝保持红热
.锥形瓶中还可观察到的现象是:
有红棕色气体产生
有红棕色气体产生
.
(5)写出乙装置中氨氧化的化学方程式:
.
(6)用CH
4催化还原NO
2可以消除氮氧化物的污染.例如.
CH
4(g)+4NO
2(g)═4NO(g)+CO
2(g)+2H
2O(g)△H=-574kJ?mol
-1,
CH
4(g)+4NO(g)═2N
2(g)+CO
2(g)+2H
2O(g)△H=-1160kJ?mol
-1,
写出CH
4还原NO
2至N
2的热化学方程式
CH4(g)+2N02(g)=N2(g)+C02(g)+2H20(g)△H=-867KJ/mol
CH4(g)+2N02(g)=N2(g)+C02(g)+2H20(g)△H=-867KJ/mol
;若用标准状况下4.48LCH
4还原NO
2至N
2整个过程中转移的电子总数为
1.6NA
1.6NA
(阿伏加德罗常数的值用N
2表示),放出的热量为
173.4
173.4
kJ.