
题目列表(包括答案和解析)
丰富多彩的化学物质不断改变着人类的生活,它们所产生的作用与其分子结构密切相关。
(1)请根据以下化合物的分子结构,回答下列问题:

①上述化合物可能的应用是________。
A.化合物(Ⅰ)可作为制造聚四氟乙烯塑料的原料;化合物(Ⅱ)可用来合成人造纤维
B.两者均可作为食品添加剂
C.两者均可作为表面活性剂,起到乳化、增溶、消泡等作用
D.两者均可用作中和胃酸的药物
②上述两个化合物进入环境后,更难被降解的是________。
(2)有三种高分子材料,结构单元如下:

请回答下列问题:
①根据上述高分子结构,能够作为高吸水性树脂的是________,其可能的理由是______________________;可作为弹性橡胶的是________,理由是________________________________________________________________________。
②有关上述高分子材料的下列说法正确的是________(可多选)。
A.高分子(Ⅴ)的单体有4种
B.高分子(Ⅲ)焚烧后产生的废气毒性最小
C.都能作为食品包装材料
D.它们的废弃物都可以回收利用
“化学与生活”模块
请在标有序号的空白处填空,并将序号及相应答案写在答题纸上:
丰富多彩的化学物质不断改变着人类的生活,它们所产生的作用与其分子结构密切相关。
(1)请根据以下化合物的分子结构,回答下列问题:
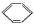
(Ⅱ)
1)上述化合物可能的应用是____________________。
A.化合物(Ⅰ)可作为制造聚四氟乙烯塑料的原料;化合物(Ⅱ)可用来合成人造纤维
B.两者均可作为食品添加剂
C.两者均可作为表面活性剂,起到乳化、增溶、消泡等作用
D.两者均可用作中和胃酸的药物
2)上述两个化合物进入环境后,更难被降解的是____________。
(2)有三种高分子材料,结构单元如下:
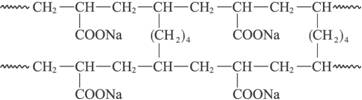
(Ⅲ)
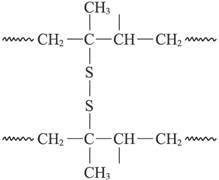
(Ⅳ)
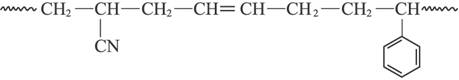
(Ⅴ)
请回答下列问题:
1)根据上述高分子结构,能够作为高吸水性树脂的是____________,其可能的理由是____________;可作为弹性橡胶的是____________,理由是____________。
2)有关上述高分子材料的下列说法正确的是____________(可多选)。
A.高分子(Ⅴ)的单体有4种
B.高分子(Ⅲ)焚烧后产生的废气毒性最小
C.都能作为食品包装材料
D.它们的废弃物都能回收利用
(1)据测算,地球上的氧气90%来自于藻类植物的光合作用,而环境污染的加剧,使海洋表层的浮游植物大量死亡,从而进一步加剧温室效应,这是由于大量浮游植物的死亡会使大气中的________________增加所致。
我国首创的铝、空气、海水电池为能源的新型海水标志灯研制成功。这种灯以海水为电解质,靠空气中的氧使铝不断氧化而产生电流。
(2)上述新型电池________________为负极,正极的电极反应式为
__________________________________________________________。
(3)自然界存在的铝矿物主要有铝土矿,它是含有少量氧化铁和石英等杂质的氧化铝,工业上制备单质铝需要纯净的氧化铝,试写出以铝土矿、海水、贝壳(主要成分为碳酸钙)为原料提纯氧化铝的化学方程式。要求只写含有铝的化合物参加的化学反应方程式,按离子反应的要求写出离子方程式。
|
下列说法错误的是 | |
| [ ] | |
A. |
化学给人类社会带来了巨大进步,但若使用不当也会给人带来危害 |
B. |
化学的任务只是研究自然界已经存在的物质,而不能根据人类的要求创造新物质 |
C. |
从远古时代起人类已开始使用化学技术 |
D. |
化学为人类社会的发展提供了丰富的物质基础 |
| A、①②③④⑥ | B、②③④⑤⑦ | C、①②④⑤⑥ | D、①③④⑦⑧ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com