
题目列表(包括答案和解析)
物质在水溶液中有不同的行为。按要求回答下列问题:
(1)Na2SO3溶液显碱性,其原因是______________________________(用离子方程式表示),该溶液中各离子浓度由大到小的顺序为______________________。
(2)室温下向10mL氨水溶液中加水稀释后,下列量增大的有__________(填编号,下同),减小的有___________,不变的有____________。
a.溶液中离子浓度? ??????? b.氨水的电离程度
c.水的离子积常数????????? d.c(H+)/ c(NH3·H2O)
(3)亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。NaClO2变质可分解为NaClO3和NaCl。取等质量已变质和未变质的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量??????????????? (填“相同”或“不相同”),其原因是??????????????????????????????????? 。
物质在水溶液中有不同的行为。按要求回答下列问题:
(1)Na2SO3溶液显碱性,其原因是______________________________(用离子方程式表示),该溶液中各离子浓度由大到小的顺序为______________________。
(2)室温下向10mL氨水溶液中加水稀释后,下列量增大的有__________(填编号,下同),减小的有___________,不变的有____________。
a.溶液中离子浓度 b.氨水的电离程度
c.水的离子积常数 d.c(H+)/ c(NH3·H2O)
(3)亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。NaClO2变质可分解为NaClO3和NaCl。取等质量已变质和未变质的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量 (填“相同”或“不相同”),其原因是 。
碱存在下,卤代烃与醇反应生成醚(R-O-R‘):
KOH
R-X + R‘OH ---→ R-O-R ’ +HX
室温
化合物 A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下:
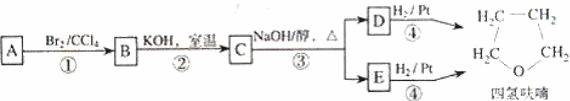
请回答下列问题:
(1)1molA和 1molH2 在一定条件下恰好反应,生成饱和一元醇 Y,Y中碳元素的质量
分数约为 65%,则 Y的分子式为 _____________________。
A分子中所含官能团的名称是 _________________。
A的结构简式为 _________________。
(2)第①②步反应类型分别为① ______________② ________________。
(3)化合物 B具有的化学性质(填写字母代号)是 __________________。
a. 可发生氧化反应 b.强酸或强碱条件下均可发生消去反应
b. 可发生酯化反应 d.催化条件下可发生加聚反应
(4)写出 C、D和 E的结构简式:
C ______________、D和 E __________________。
(5)写出化合物 C与 NaOH水溶液反应的化学方程式:
__________________________________________________
(6)写出四氢呋喃链状醚类的所有同分异构体的结构简式:
________________________________.
| |||||||||||||||||||||||||||||||||||||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com