
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
ўс. ЈЁ1Ј©Л®·ЦЧУөДБўМеҪб№№КЗ Ј¬Л®·ЦЧУДЬУләЬ¶аҪрКфАлЧУРОіЙЕдәПОпЈ¬ЖдФӯТтКЗФЪСхФӯЧУЙПУР ЎЈ
ЈЁ2Ј©ұщҫ§°ыЦРЛ®·ЦЧУөДҝХјдЕЕБР·ҪКҪУлҪрёХКҜҫ§°ыЈЁЖдҫ§°ыҪб№№ИзУТНјЈ¬ЖдЦРҝХРДЛщКҫФӯЧУО»УЪБў·ҪМеөД¶Ҙөг»тГжРДЈ¬КөРДЗтЛщКҫФӯЧУО»УЪБў·ҪМеДЪЈ©АаЛЖЎЈГҝёцұщҫ§°ыЖҪҫщХјУР ёцЛ®·ЦЧУЎЈұщҫ§°ыУлҪрёХКҜҫ§°ыОўБЈЕЕБР·ҪКҪПаН¬өДФӯТтКЗ ЎЈ
ЈЁ3Ј©КөСйІвөГұщЦРЗвјьөДЧчУГДЬОӘ18.5kJЎӨmolЎӘ1Ј¬¶шұщИЫ»ҜИИОӘ5.0kJЎӨmol-1Ј¬ХвЛөГч ЎЈ
ўт. ЈЁ1Ј©өвФЪІ»Н¬ИЬјБЦРіКПЦЧПЙ«ЎўЧШЙ«ЎӯЎӯТ»°гИПОӘИЬТәіКЧПЙ«өДұнГчИЬҪвБЛөДЎ°өв·ЦЧУЎұІўОҙәНИЬјБ·ўЙъәЬЗҝөДҪбәПЎЈТСЦӘІ»Н¬ОВ¶ИПВЈ¬өвФЪКҜАҜУНЦРөДИЬТәіКЧПЙ«»тЧШЙ«ЎЈЗл»ШҙрЈәОВ¶ИөНКұИЬТәіК Й«Ј¬ОВ¶ИёЯКұИЬТәіК Й«Ј¬ТтОӘ ЎЈ
ЈЁ2Ј©ФЪЛ®ҫ§өДЦщГжЙПНҝТ»ІгКҜАҜЈ¬УГәмИИөДХлҪУҙҘГжЦРСлЈ¬КҜАҜИЫ»ҜәуіКНЦФІРОЈ»УГІЈБ§ҙъМжЛ®ҫ§ЦШёҙЙПКцІЩЧчЈ¬ИЫ»ҜөДКҜАҜФтіКФІРОЎЈКФУГДгЛщС§№э№ШУЪҫ§МеРФЦКөДЦӘК¶ҪвКНЙПКцПЦПуЎЈ
ўс. ЈЁ1Ј©Л®·ЦЧУөДБўМеҪб№№КЗ Ј¬Л®·ЦЧУДЬУләЬ¶аҪрКфАлЧУРОіЙЕдәПОпЈ¬ЖдФӯТтКЗФЪСхФӯЧУЙПУР ЎЈ
ЈЁ2Ј©ұщҫ§°ыЦРЛ®·ЦЧУөДҝХјдЕЕБР·ҪКҪУлҪрёХКҜҫ§°ыЈЁЖдҫ§°ыҪб№№ИзУТНјЈ¬ЖдЦРҝХРДЛщКҫФӯЧУО»УЪБў·ҪМеөД¶Ҙөг»тГжРДЈ¬КөРДЗтЛщКҫФӯЧУО»УЪБў·ҪМеДЪЈ©АаЛЖЎЈГҝёцұщҫ§°ыЖҪҫщХјУР ёцЛ®·ЦЧУЎЈұщҫ§°ыУлҪрёХКҜҫ§°ыОўБЈЕЕБР·ҪКҪПаН¬өДФӯТтКЗ ЎЈ
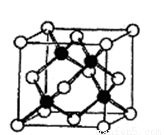
ЈЁ3Ј©КөСйІвөГұщЦРЗвјьөДЧчУГДЬОӘ18.5kJЎӨmolЎӘ1Ј¬¶шұщИЫ»ҜИИОӘ5.0kJЎӨmol-1Ј¬ХвЛөГч ЎЈ
ўт. ЈЁ1Ј©өвФЪІ»Н¬ИЬјБЦРіКПЦЧПЙ«ЎўЧШЙ«ЎӯЎӯТ»°гИПОӘИЬТәіКЧПЙ«өДұнГчИЬҪвБЛөДЎ°өв·ЦЧУЎұІўОҙәНИЬјБ·ўЙъәЬЗҝөДҪбәПЎЈТСЦӘІ»Н¬ОВ¶ИПВЈ¬өвФЪКҜАҜУНЦРөДИЬТәіКЧПЙ«»тЧШЙ«ЎЈЗл»ШҙрЈәОВ¶ИөНКұИЬТәіК Й«Ј¬ОВ¶ИёЯКұИЬТәіК Й«Ј¬ТтОӘ ЎЈ
ЈЁ2Ј©ФЪЛ®ҫ§өДЦщГжЙПНҝТ»ІгКҜАҜЈ¬УГәмИИөДХлҪУҙҘГжЦРСлЈ¬КҜАҜИЫ»ҜәуіКНЦФІРОЈ»УГІЈБ§ҙъМжЛ®ҫ§ЦШёҙЙПКцІЩЧчЈ¬ИЫ»ҜөДКҜАҜФтіКФІРОЎЈКФУГДгЛщС§№э№ШУЪҫ§МеРФЦКөДЦӘК¶ҪвКНЙПКцПЦПуЎЈ
ДҝЗ°Ј¬И«КАҪзДшөДПы·СБҝҪцҙОУЪНӯЎўВБЎўЗҰЎўРҝЈ¬ҫУУРЙ«ҪрКфөЪОеО»ЎЈДшРРТө·ўХ№ФМІШЧЕҫЮҙуЗұБҰЎЈ
ЈЁ1Ј©ЕдәПОпNi(CO)4іЈОВОӘТәМ¬Ј¬ТЧИЬУЪCCl4ЎўұҪөИУР»ъИЬјБЎЈ№ММ¬Ni(CO)4КфУЪ ҫ§МеЈ»»щМ¬NiФӯЧУөДөзЧУЕЕІјКҪОӘ Ј¬РҙіцУлCO»ҘОӘөИөзЧУМеөДТ»ЦЦАлЧУөД»ҜС§КҪОӘ ЎЈ
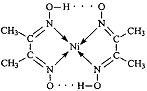 ЈЁ2Ј©УТНјЕдәПОп·ЦЧУДЪөДЧчУГБҰіэ№ІјЫјьНвЈ¬»№ҙжФЪөДБҪЦЦЧчУГ БҰКЗ ЈЁМоұаәЕЈ©ЎЈ
ЈЁ2Ј©УТНјЕдәПОп·ЦЧУДЪөДЧчУГБҰіэ№ІјЫјьНвЈ¬»№ҙжФЪөДБҪЦЦЧчУГ БҰКЗ ЈЁМоұаәЕЈ©ЎЈ
A.Звјь B.АлЧУјь C. ·¶өВ»ӘБҰ D.ЕдО»јь
ЈЁ3Ј©әЬ¶аІ»ұҘәНУР»ъОпФЪNiҙЯ»ҜПВҝЙТФУлH2·ўЙъјУіЙ·ҙУҰЎЈ
ИзЈәўЩCH2=CH2ЎўўЪCHЎФCHЎўўЫ![]() ЎўўЬHCHOөИЈ¬ЖдЦРМјФӯЧУІЙИЎsp2ФУ»ҜөД·ЦЧУУР ЈЁМоОпЦКРтәЕЈ©Ј¬HCHO·ЦЧУөДБўМеҪб№№ОӘ РОЎЈ
ЎўўЬHCHOөИЈ¬ЖдЦРМјФӯЧУІЙИЎsp2ФУ»ҜөД·ЦЧУУР ЈЁМоОпЦКРтәЕЈ©Ј¬HCHO·ЦЧУөДБўМеҪб№№ОӘ РОЎЈ
ЈЁ4Ј©MnЎўFeәНNiТ»СщҫщОӘөЪЛДЦЬЖЪ№э¶ЙФӘЛШЈ¬БҪФӘЛШөДІҝ·ЦөзАлДЬКэҫЭИзПВұнЎЈ
| ФӘ ЛШ | Mn | Fe | |
| өзАлДЬ /kJЎӨmolЈӯ1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
ҫЭҙЛ·ЦОцMn2+ұИFe2+ ЈЁМо Ў°ёьТЧЎұ »тЎ°ёьДС ЎұЈ©ФЩК§ИҘЈӯёцөзЧУЈ¬ҙУОўБЈҪб№№өДҪЗ¶ИјтКцЖдФӯТтКЗ ЎЈ
ЈЁ5Ј©NiOөДҫ§МеҪб№№АаРНУлВИ»ҜДЖөДПаН¬Ј¬NiOҫ§°ыЦРУлNiЧоҪьөДNiөДКэДҝОӘ ёцЎЈ
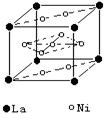 ЈЁ6Ј©ЗвЖшКЗРВРНЗеҪаДЬФҙЈ¬пзЈЁLaЈ©әНДшөДәПҪрҝЙЧцҙўЗвІДБПЎЈёГәПҪрөДҫ§°ыИзНјЛщКҫЈ¬ҫ§°ыЦРРДУРТ»ДшФӯЧУЈ¬ЖдЛыДшФӯЧУ¶јФЪҫ§°ыГжЙПЎЈёГҫ§МеөД»ҜС§КҪКЗ______ЎЈ
ЈЁ6Ј©ЗвЖшКЗРВРНЗеҪаДЬФҙЈ¬пзЈЁLaЈ©әНДшөДәПҪрҝЙЧцҙўЗвІДБПЎЈёГәПҪрөДҫ§°ыИзНјЛщКҫЈ¬ҫ§°ыЦРРДУРТ»ДшФӯЧУЈ¬ЖдЛыДшФӯЧУ¶јФЪҫ§°ыГжЙПЎЈёГҫ§МеөД»ҜС§КҪКЗ______ЎЈ
ПЦУРAЎўBЎўCЎўDЛДЦЦ¶МЦЬЖЪФӘЛШЈ¬ЛьГЗөДПа№ШҪб№№әНРФЦКРЕПўИзПВұнЛщКҫЈ¬ЗлҪбәППа№ШРЕПўЈ¬НкіЙПа№ШөДОКМвЈә
ФӘЛШ Па№ШҪб№№әНРФЦК
A ЖдөҘЦКөДТ»ЦЦҫ§МеІ»КЗҪрКфҫ§МеЈ¬ө«КЗөзөДБјөјМеЈ¬ЗТДСИЫЎўЦКИнІўУРИу»¬РФЈ¬ҝЙУГЧчФӯЧУәЛ·ҙУҰ¶СөДВэ»ҜјБЎў»рјэ·ў¶Ҝ»ъЕз№аәНөзј«ІДБПөИЎЈ
B ЖдөҘЦКјИДЬУлЗҝЛбИЬТә·ҙУҰЈ¬УЦДЬУлЗҝјоИЬТә·ҙУҰЈ¬ЖдјтөҘАлЧУФЪөЪИэЦЬЖЪөҘәЛАлЧУЦР°лҫ¶ЧоРЎЎЈ
C КЗө°°ЧЦКөДЧйіЙФӘЛШЦ®Т»Ј¬ФӯЧУәЛНвУРИэЦЦІ»Н¬ДЬБҝөДөзЧУЈ¬ЗТОҙіЙ¶ФөзЧУКэЧо¶аЎЈ
D ФӯЧУәЛНвЧоНвІгөзЧУЕЕІјКҪОӘnsnnp2n+1
ЈЁ1Ј©ұнЦРЛщКцAөДөҘЦКҫ§МеЦРОўБЈјдөДПа»ҘЧчУГУР_____________Ўў_____________ЎЈ
ЈЁ2Ј©BФӘЛШөДСх»ҜОпЛщ¶ФУҰөДҫ§МеКфУЪ____ҫ§МеЈЁМоЎ°·ЦЧУЎұЎўЎ°ФӯЧУЎұЎўЎ°АлЧУЎұЎўЎ°ҪрКфЎұЈ©Ј¬№ӨТөЙПЦЖұёBФӘЛШөҘЦКөД»ҜС§·ҪіМКҪЈә_______________________ЎЈ
ЈЁ3Ј©ДЖУлCФӘЛШРОіЙөДNa3Cҫ§МеЦРЈ¬CФӘЛШТФC3-ҙжФЪЈ¬C3-өДөзЧУЕЕІјКҪОӘ_____________ЎЈCФӘЛШөДЖшМ¬Зв»ҜОпИЬУЪЛ®әуИЬТәіКјоРФөДФӯТтЈЁУГ·ҪіМКҪұнКҫЈ©_____________ЈЁМоРтәЕЈ©ЎЈ
ЈЁ4Ј©УлDН¬ЦчЧеөД¶МЦЬЖЪФӘЛШЈ¬ЖдөҘЦКј°Жд»ҜәПОпУлDөДөҘЦКј°»ҜәПОпҫщҫЯУРөДРФЦКОӘ____ ЈЁМоРтәЕЈ©ЎЈ
AЈ®іЈОВПВөҘЦКёъЛ®ҫзБТ·ҙУҰІў·ЕіцСхЖш BЈ®ЖшМ¬өӘ»ҜОпҫЯУРәЬЗҝөДИИОИ¶ЁРФ
CЈ®ЖшМ¬Зв»ҜОпј«ТЧИЬУЪЛ®ІўіКЗҝЛбРФ DЈ®ФЪHXOЦРXөД»ҜәПјЫҫщОӘ+lјЫ
| ФӘЛШ | Па№ШҪб№№әНРФЦК |
| A | ЖдөҘЦКөДТ»ЦЦҫ§МеІ»КЗҪрКфҫ§МеЈ¬ө«КЗөзөДБјөјМеЈ¬ЗТДСИЫЎўЦКИнІўУРИу»¬РФЈ¬ҝЙУГЧчФӯЧУәЛ·ҙУҰ¶СөДВэ»ҜјБЎў»рјэ·ў¶Ҝ»ъЕз№аәНөзј«ІДБПөИЎЈ |
| B | ЖдөҘЦКјИДЬУлЗҝЛбИЬТә·ҙУҰЈ¬УЦДЬУлЗҝјоИЬТә·ҙУҰЈ¬ЖдјтөҘАлЧУФЪөЪИэЦЬЖЪөҘәЛАлЧУЦР°лҫ¶ЧоРЎЎЈ |
| C | КЗө°°ЧЦКөДЧйіЙФӘЛШЦ®Т»Ј¬ФӯЧУәЛНвУРИэЦЦІ»Н¬ДЬБҝөДөзЧУЈ¬ЗТОҙіЙ¶ФөзЧУКэЧо¶аЎЈ |
| D | ФӯЧУәЛНвЧоНвІгөзЧУЕЕІјКҪОӘnsnnp2n+1 |
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com