
题目列表(包括答案和解析)
(1)A为_________元素,B为_________元素;C为__________元素。D的质子数和中子数相等,D的原子组成符号为_________,它的最高价为_______价。
(2)用电子式表示A、D两元素形成AD2的过程:______________________________,用电子式表示C、D两元素形成化学键的过程:______________________________。
(3)写出E和A的最高价氧化物反应的化学方程式:________________________________。
(10分)A、B、C、D四种元素的原子序数均小于18,其最高正价数依次为1,4,5,7,已知B的原子核外次外层电子数为2。A、C原子的核外次外层电子数为8。D元素的最高价氧化物对应的水化物是已知含氧酸中最强酸,则:
(1)A的离子结构示意图是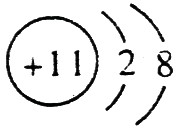 ,C的原子结构示意图是
,C的原子结构示意图是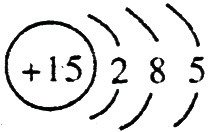 。
。
(2)C的最高价氧化物对应的水化物与A的氢氧化物生成三种盐,化学式分别为Na3PO4、Na2HPO4、NaH2PO4。
(3)C、D的气态氢化物稳定性由强到弱的顺序是 HCl>PH3。
【解析】 最高正价=原子最外层电子数,B元素的原子最外层电子数应为4,B元素原子的次外层电子数为2,为K层,B元素原子核外共有2+4=6个电子,B是6号元素碳;A、C原子次外层电子数为8,则A、C原子核外电子数分别是:2+8+1=11和2+8+5=15,所以A为11号元素钠,C为15号元素磷;在1~18号元素中,最高价为+7的只有氯元素(F无正价),而HClO4是已知含氧酸中最强的酸,故D为氯。
(1)钠总是+1价,其离子结构示意图为: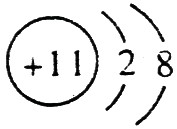 ;磷的原子序数是15,其原子结构示意图是:
;磷的原子序数是15,其原子结构示意图是: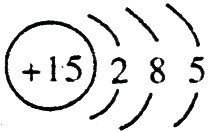 。
。
(2)磷的最高价(+5)氧化物对应的水化物是H3PO4,与NaOH反应生成:Na3PO4、NaH2PO4三种盐。
(3)P、Cl原子都具有3个电子层,核电荷数P(15)小于Cl(17),原子半径r(P)>r(Cl),所以非金属Cl>P,气态氢化物稳定性HCl>PH3。
(1)A、B、C、D分别是___________、___________、___________、___________。
(2)A的离子结构示意图为________________,C的原子结构示意图为________________。
(3)C的最高价氧化物对应的水化物与A的氢氧化物可生成___________种盐,其化学式分别为___________、___________、___________、___________。(可不填满,也可补充)
(4)C、D的气态氢化物稳定性由强到弱的顺序为____________。
(1)A、B、C、D分别是___________、___________、___________、___________。
(2)A离子的结构示意图为___________。
(3)C原子的结构示意图为___________。
(4)C的最高价氧化物对应水化物与A的氢氧化物反应最多生成___________种盐,其化学式为______________________。
(5)C、D的气态氢化物稳定性由强到弱的顺序为______________________。
(1)A、B、C、D分别是_____________、_____________、_____________、_____________。
(2)A的离子结构示意图为_____________,C的原子结构示意图为_____________。
(3)C的最高价氧化物对应的水化物与A的氢氧化物生成_____________种盐,其化学式为_________________________________________________________________。
(4)C、D的气态氢化物稳定性由强到弱的顺序是_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com