X、Y、Z和W为原子序数依次增大的短周期元素,X是空气中含量最高的元素,Y 和Z同主族,Z和W的气态氢化物具有相同的电子数,Y的单质只有氧化性.
(1)写出Z的气态氢化物的结构式
H-S-H
H-S-H
,与W同周期惰性气体元素的原子结构示意图
.
(2)写出用惰性电极电解Cu(XY
3)
2溶液的离子反应方程式
.
(3)某小组设计如图1所示的装置图(图中夹持和加热装置略去),分别研究ZY
2和W
2的性质.
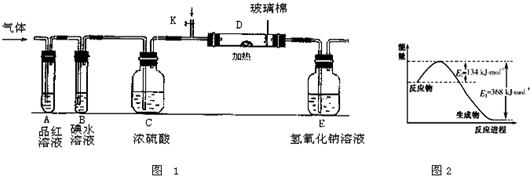
①分别通入ZY
2和W
2,在装置A中观察到的现象是否相同(填“相同”或“不相同”)
相同
相同
;
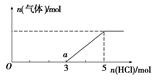
②若装置B中装有5.0mL 1.0×10
-3mol/L的碘水,当通入足量W
2完全反应后,转移的电子为5.0×10
-5mol,则该反应的化学方程式为
5Cl2+I2+6H2O=2HIO3+10HCl
5Cl2+I2+6H2O=2HIO3+10HCl
.
(4)某同学将足量的ZY
2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量(填字母)
AC
AC
,可以看到白色沉淀生成,其原因为:
当加入氨水时,使该溶液变为碱性,产生BaSO3白色沉淀(或当加入HNO3时,使溶液中H2SO3氧化成H2SO4,产生BaSO4白色沉淀)
当加入氨水时,使该溶液变为碱性,产生BaSO3白色沉淀(或当加入HNO3时,使溶液中H2SO3氧化成H2SO4,产生BaSO4白色沉淀)
(写出其中一种即可).
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙
(5)图2是1molXO
2和1molCO反应生成CO
2和XO过程中能量变化示意图,请写出XO
2和CO反应的热化学方程式
NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ?mol-1
NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ?mol-1
.
(6)盐酸肼(X
2H
6Cl
2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与XH
4Cl类似.
写出盐酸肼第一步水解反应的离子方程式
N2H62++H2O?[N2H5?H2O]++H+
N2H62++H2O?[N2H5?H2O]++H+
.

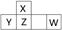


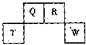 (2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题: