
题目列表(包括答案和解析)
2CO(g)+O2(g)====2CO2(g) ΔH=-566 kJ·mol-1
CH4(g)+2O2(g)====CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
又知由H2与O2反应生成液态H2O比生成气态H2O多放出44 kJ·mol-1的热量。下列CH4气体在空气中不完全燃烧时的热化学方程式中正确的是
A.2CH4(g)+![]() O2(g)====CO2(g)+CO(g)+4H2O(l) ΔH=-1 214 kJ·mol-1
O2(g)====CO2(g)+CO(g)+4H2O(l) ΔH=-1 214 kJ·mol-1
B.2CH4(g)+![]() O2(g)====CO2(g)+CO(g)+4H2O(g) ΔH=-1 038 kJ·mol-1
O2(g)====CO2(g)+CO(g)+4H2O(g) ΔH=-1 038 kJ·mol-1
C.3CH4(g)+5O2(g)====CO2(g)+2CO(g)+6H2O(l) ΔH=-1 538 kJ·mol-1
D.3CH4(g)+5O2(g)====CO2(g)+2CO(g)+6H2O(g) ΔH=-1 840 kJ·mol-1
在一定条件下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g) 2CO2(g); △H=-566kJ·mol-1
CH4(g)+2O2(g) CO2(g)+2H2O(1); △H=-890kJ·mol-1
又知由H2与O2反应生成液态H2O 比生成气态H2O 多放出44kJ/mol的热量。则CH4 气体在空气中不完全燃烧热化学方程式正确的是
A.2CH4(g)+O2(g) CO2(g)+CO(g)+4H2O(1) △H=-1214kJ·mol-1
B.2CH4(g)+O2(g) CO2(g)+CO(g)+4H2O(g) △H=-1038kJ·mol-1
C.3CH4(g)+5O2(g) CO2(g)+2CO(g)+6H2O(1) △H=-1538kJ·mol-1
D.3CH4(g)+5O2(g) CO2(g)+2CO(g)+6H2O(g) △H=-1840kJ·mol-1
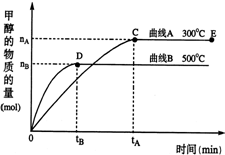 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)| c(CH3OH) |
| c(CO)?C2(H2) |
| c(CH3OH) |
| c(CO)?C2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| 1 |
| 2 |
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)

根据题意完成下列各小题:
⑴反应达到平衡时,平衡常数表达式K=______,升高温度,K值____(填“增大”、“减小”、“不变”)。
⑵在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=__________________。
(用上图中出现的字母表示)
⑶在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是______________________。
a.氢气的浓度减小 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
⑷据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:_________________________(用化学方程式表示)。
⑸能源问题是人类社会面临的重大课题,甲醇是未来的重要的能源物质。常温下,1g甲醇完全燃烧生成液态水时放出22.7kJ的能量,写出甲醇燃烧热的热化学方程式__________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com