
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
дкБъзМзДПіЯТЃЌ560ЬхЛ§АБЦјШмгк1ЬхЛ§ЕФЫЎжаЃЌВтЕУАБЫЎЕФУмЖШЮЊ0.9gЁЄcmЃ3ЃЌдђАБЫЎЕФЮяжЪЕФСПХЈЖШЮЊ
[ЁЁЁЁ]
ЙЄвЕЩЯГЃгУЬњжЪШнЦїЪЂзАРфХЈСђЫсЃЎЮЊбаОПЬњжЪВФСЯгыШШХЈСђЫсЕФЗДгІЃЌФГбЇЯАаЁзщНјааСЫвдЯТЬНОПЛюЖЏЃК
[ЬНОПвЛ]
(1)НЋвбШЅГ§БэУцбѕЛЏЮяЕФЬњЖЄ(ЬМЫиИж)ЗХШыРфХЈСђЫсжаЃЌ10ЗжжгКѓвЦШыСђЫсЭШмвКжаЃЌЦЌПЬКѓШЁГіЙлВьЃЌЬњЖЄБэУцЮоУїЯдБфЛЏЃЌЦфдвђЪЧ________
(2)СэГЦШЁЬњЖЄ6.0 gЗХШы15.0 mLХЈСђЫсжаЃЌМгШШЃЌГфЗжЗДгІКѓЕУЕНШмвКXВЂЪеМЏЕНЦјЬхYЃЎ
ЂйМзЭЌбЇШЯЮЊXжаГ§Fe3+жЎЭтЛЙПЩФмКЌгаFe2+ЃЎШєвЊШЗШЯЦфжаЕФFe2+ЃЌгІбЁгУ________(ЬюађКХ)ЃЎ
AЃЎKSCNШмвККЭТШЫЎ
BЃЎЬњЗлКЭKSCNШмвК
CЃЎХЈАБЫЎ
DЃЎЫсадKMnO4ШмвК
ЂкввЭЌбЇШЁ560 mL(БъзМзДПі)ЦјЬхYЭЈШызуСПфхЫЎжаЃЌЗЂЩњSO2ЃЋBr2ЃЋ2H2O
ЃН2HBrЃЋH2SO4ЗДгІЃЌШЛКѓМгШызуСПBaCl2ШмвКЃЌОЪЪЕБВйзїКѓЕУИЩдяЙЬЬх4.66 gЃЎгЩДЫЭЦжЊЦјЬхYжаSO2ЕФЬхЛ§ЗжЪ§ЮЊ________[ЬНОПЖў]
ЗжЮіЩЯЪіЪЕбщжаSO2ЬхЛ§ЗжЪ§ЕФНсЙћЃЌБћЭЌбЇШЯЮЊЦјЬхYжаЛЙПЩФмКЌгаH2КЭQЦјЬхЃЎЮЊДЫЩшМЦСЫЯТСаЬНОПЪЕбщзАжУ(ЭМжаМаГжвЧЦїЪЁТдЃЌМйЩшгаЙиЦјЬхЭъШЋЗДгІ)ЃЎ

(3)зАжУBжаЪдМСЕФзїгУЪЧ________
(4)ШЯЮЊЦјЬхYжаЛЙКЌгаQЕФРэгЩЪЧ________(гУЛЏбЇЗНГЬЪНБэЪО)ЃЎ
(5)ЮЊШЗШЯQЕФДцдкЃЌашдкзАжУжаЬэМгЯДЦјЦПMгк________(бЁЬюађКХ)ЃЎ
aЃЎAжЎЧА
bЃЎAЃBМф
cЃЎBЃCМф
dЃЎCЃDМф
(6)ШчЙћЦјЬхYжаКЌгаH2ЃЌдЄМЦЪЕбщЯжЯѓгІЪЧ________
ЃЈ12ЗжЃЉЮЊбаОПЬњжЪВФСЯгыШШХЈСђЫсЕФЗДгІЃЌФГбЇЯАаЁзщгУЬМЫиИж(МДЬњКЭЬМЕФКЯН№)НјааСЫвдЯТЬНОПЛюЖЏЃК
[ЬНОПвЛ]ЃЈ1ЃЉНЋвбШЅГ§БэУцбѕЛЏЮяЕФЬњЖЄ(ЬМЫиИж)ЗХШыРфХЈСђЫсжаЃЌ10ЗжжгКѓвЦШыСђЫсЭШмвКжаЃЌЦЌПЬКѓШЁГіЙлВьЃЌЬњЖЄБэУцЮоУїЯдБфЛЏЃЌЦфдвђЪЧ ЁЃ
ЃЈ2ЃЉГЦШЁЬМЫиИж6ЃЎ0 gЗХШы15ЃЎ0 mLХЈСђЫсжаЃЌМгШШЃЌГфЗжЗДгІКѓЕУЕНШмвКXВЂЪеМЏЕНЛьКЯЦјЬхYЁЃ
ЂйМзЭЌбЇШЯЮЊXжаГ§Fe3ЃЋжЎЭтЛЙПЩФмКЌгаFe2ЃЋЁЃШєвЊШЗШЯЦфжаЕФFe2ЃЋЃЌгІбЁгУ (бЁЬюађКХ)ЁЃ
AЃЎKSCNШмвККЭТШЫЎ BЃЎЬњЗлКЭKSCNШмвК
CЃЎХЈАБЫЎ DЃЎЫсадKMnO4ШмвК
ЂкввЭЌбЇШЁ560 mL(БъзМзДПі)ЦјЬхYЭЈШызуСПфхЫЎжаЃЌШЛКѓМгШызуСПBaCl2ШмвКЃЌОЪЪЕБВйзїКѓЕУИЩдяЙЬЬх4ЃЎ66 gЁЃгЩДЫЭЦжЊЦјЬхYжаSO2ЕФЬхЛ§ЗжЪ§ЮЊ ЁЃ
[ЬНОПЖў]ИљОнЩЯЪіЪЕбщжаSO2ЬхЛ§ЗжЪ§ЕФЗжЮіЃЌБћЭЌбЇШЯЮЊЦјЬхYжаЛЙПЩФмКЌгаQ1КЭQ2СНжжЦјЬхЃЌЦфжаQ1ЦјЬхЃЌдкБъзМзДПіЯТЃЌУмЖШЮЊ0ЃЎ0893 gЁЄLЃ1ЁЃЮЊДЫЩшМЦСЫЯТСаЬНОПЪЕбщзАжУ(МйЩшгаЙиЦјЬхЭъШЋЗДгІ)ЁЃ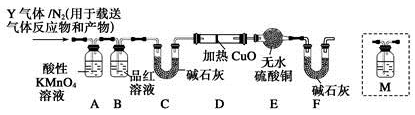
ЃЈ3ЃЉзАжУBжаЪдМСЕФзїгУЪЧ ЁЃ
ЃЈ4ЃЉЗжЮіYЦјЬхжаЕФQ2ЦјЬхЪЧШчКЮЩњГЩЕФ (гУЛЏбЇЗНГЬЪНБэЪО)ЁЃ
ЃЈ5ЃЉвбжЊЯДЦјЦПMжаЪЂзАГЮЧхЪЏЛвЫЎЃЌЮЊШЗШЯQ2ЕФДцдкЃЌашдкзАжУжаЬэМгЯДЦјЦПMгк (ЬюађКХ)ЁЃ
AЃЎAжЎЧА BЃЎAЁЊBМф
CЃЎBЁЊCМф DЃЎCЁЊDМф
ЃЈ6ЃЉШчЙћЦјЬхYжаКЌгаQ1ЃЌдЄМЦЪЕбщЯжЯѓгІЪЧ ЁЃ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com