
题目列表(包括答案和解析)
将一定质量的金属钠在空气中燃烧并将固体产物跟338g水反应,收集到16g气体,下列说法正确的是
A.原金属钠的质量是11.5 g B.原金属钠的质量是46 g
C.所得溶液中溶质的质量分数为20% D.所得溶液中溶质的质量分数为21.1%
 (1)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
(1)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:(10分)(1)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
①通甲烷的铂丝为原电池的______极,发生的电极反应为____________________。
②该电池工作时(放电)反应的总化学方程式为_______________________________。
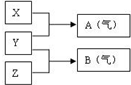
(2)X、Y、Z为三种不同短周期非金属元素的单质。在一定条件下发生如下反应: 若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式为 ;
②向苛性钠溶液中通入过量的A所发生反应的离子方程式为
③将B与氯气的水溶液充分反应可生成两种强酸,该反应的化学方程式为
(10分)(1)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
①通甲烷的铂丝为原电池的______极,发生的电极反应为____________________。
②该电池工作时(放电)反应的总化学方程式为_______________________________。
(2)X、Y、Z为三种不同短周期非金属元素的单质。在一定条件下发生如下反应: 若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则: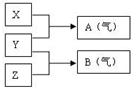
①B的化学式为 ;
②向苛性钠溶液中通入过量的A所发生反应的离子方程式为
③将B与氯气的水溶液充分反应可生成两种强酸,该反应的化学方程式为
(10分)(1)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
①通甲烷的铂丝为原电池的______极,发生的电极反应为____________________。
②该电池工作时(放电)反应的总化学方程式为_______________________________。
(2)X、Y、Z为三种不同短周期非金属元素的单质。在一定条件下发生如下反应: 若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
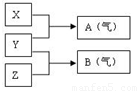
①B的化学式为 ;
②向苛性钠溶液中通入过量的A所发生反应的离子方程式为
③将B与氯气的水溶液充分反应可生成两种强酸,该反应的化学方程式为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com