
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
ҪрКфёҜКҙФміЙәЬҙуөДҫӯјГЛрК§Ј¬ЙхЦБі¬№эЧФИ»ФЦәҰЈ¬ЖдЦРёЦМъРвКҙЧоОӘСПЦШЈ¬С°Зу·АЦ№ёЦМъёҜКҙөД·Ҫ·ЁТвТеЦШҙуЎЈ
ЈЁ1Ј©ёЦМъөДұнГж·ўА¶Ўў·ўәЪҙҰАнКЗіЈУГөД·АёҜ·Ҫ·ЁЎЈПВБР·ҙУҰКЗЦчТӘ·ҙУҰЦ®Т»ЎЈ
ЗлЕдЖҪ·ҪіМКҪЈәҝЪ Na2FeO2+ ҝЪ NaNO2+ ҝЪ = ҝЪ NaFeO2+ ҝЪ NH3Ўь+ ҝЪ NaOH
ЈЁ2Ј©ёЦМъөДЎ°¶Ы»ҜЎұҙҰАнТІДЬҙпөҪ·АёҜДҝөДЈ¬ҫӯАдЎўЕЁ HNO3 ҙҰАнәуЈ¬ЖдұнГжУРТ»ІгЦВГЬСх»ҜОпұЈ»ӨДӨЈ¬ө«КЗјУИИ»тФЪПЎHNO3ЦР ҫНІ»ДЬ Ў°¶Ы»ҜЎұЎЈІ»Н¬ЕЁ¶ИөДHNO3 УлМъ·ҙУҰөД»№ФӯІъОпәЬёҙФУЈ¬Жд·ЦІјЗъПЯИзНјЎЈ
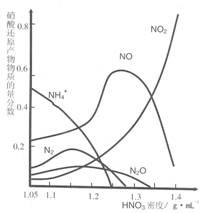
ўЩНјКҫҝЙЦӘЈ¬ГЬ¶ИОӘ 1.05g?mLЈӯ1 өДПхЛбУлМъ·ҙУҰКұЈ¬ЖдЧо¶аөД»№ФӯІъОпКЗ
Ј»ГЬ¶ИҙуУЪ1.35 g?mLЈӯ1өДПхЛбУлМъ·ҙУҰКұЈ¬Жд»№ФӯІъОпЦчТӘКЗ NO2Ј»·ЦОцHNO3 УлМъ·ҙУҰөД№жВЙКЗЈә ЎЈ
ўЪ mg МъУлә¬ n g HNO3өДПхЛбИЬТәЗЎәГНкИ«·ҙУҰЈ¬ИфПхЛбөД»№ФӯІъОпЦ»УР NO, Фт m өДИЎЦөҝЙДЬКЗ (МоЧЦДёұаәЕ )
AЈ®![]() BЈ®
BЈ®![]() CЈ®
CЈ®![]() DЈ®
DЈ®![]() EЈ®
EЈ®![]()
ўЫ№ӨТөЙПТ»°гІ»УГАдЕЁПхЛбҪшРРМъұнГжҙҰАнЈ¬ЖдҝЙДЬөДФӯТтКЗЈә
ЎЈ
ЈЁ3Ј©ҪрКф (M) өДёҜКҙКЗТтОӘ·ўЙъ·ҙУҰЈә MЈӯneЈӯЎъMn+Ј¬іэБЛЙПКцұнГжҙҰАнөД·Ҫ·ЁНвЈ¬ПВБР·Ҫ·ЁТІДЬЖрөҪ·АёҜЧчУГөДКЗ ЈЁМоЧЦДёұаәЕЈ©
AЈ®ФЪМъЦРІфИлГъЎўХтөИҪрКфЈ¬ёДұдЖдДЪІҝҪб№№Ј¬ЦЖіЙІ»РвёЦ
BЈ®ФЪМъЦЖЖ·ұнГж¶ЖҙЗ
CЈ®МбёЯМъЦРә¬МјБҝЈ¬ЦЖіЙЙъМъ
DЈ®Ҫ«Л®ҝвМъХўГЕУлЦұБчөзФҙөДёәј«ПаБ¬

ҪрКф | өзЧУБч¶Ҝ·ҪПт | өзС№/V |
A | AЎъCu | +0.78 |
B | CuЎъB | Јӯ0.15 |
C | CЎъCu | +1.35 |
D | DЎъCu | +0.30 |
ТСЦӘЈә№№іЙБҪөзј«өДҪрКф»оЖГРФПаІоФҪҙуЈ¬өзС№ұнөД¶БКэФҪҙуЎЈ
ЗлТАҫЭұнЦРКэҫЭЕР¶ПЈә
(1)___________ҪрКфҝЙДЬКЗЧоЗҝөД»№ФӯјБЈ»___________ҪрКфТ»¶ЁІ»ДЬҙУБтЛбНӯИЬТәЦРЦГ»»іцНӯЎЈ
(2)ИфВЛЦҪІ»УГСОИЬТәҪюИу¶шёДУГNaOHИЬТәҪюИуЈ¬ФтФЪВЛЦҪЙПДЬҝҙөҪУРА¶Й«іБөнОціцөДКЗ____________(МоЧЦДё)ҪрКфЎЈЖд¶ФУҰөДФӯөзіШөДөзј«·ҙУҰКҪОӘЈә
ёәј«___________________________Ј¬Хэј«______________________________ЎЈ

ҪрКф | өзЧУБч¶Ҝ·ҪПт | өзС№/V |
A | AЎъCu | +0.78 |
B | CuЎъB | Јӯ0.15 |
C | CЎъCu | +1.35 |
D | DЎъCu | +0.30 |
ТСЦӘЈә№№іЙБҪөзј«өДҪрКф»оЖГРФПаІоФҪҙуЈ¬өзС№ұнөД¶БКэФҪҙуЎЈ
ЗлТАҫЭұнЦРКэҫЭЕР¶ПЈә
(1)___________ҪрКфҝЙДЬКЗЧоЗҝөД»№ФӯјБЈ»___________ҪрКфТ»¶ЁІ»ДЬҙУБтЛбНӯИЬТәЦРЦГ»»іцНӯЎЈ
(2)ИфВЛЦҪІ»УГСОИЬТәҪюИу¶шёДУГNaOHИЬТәҪюИуЈ¬ФтФЪВЛЦҪЙПДЬҝҙөҪУРА¶Й«іБөнОціцөДКЗ____________(МоЧЦДё)ҪрКфЎЈЖд¶ФУҰөДФӯөзіШөДөзј«·ҙУҰКҪОӘЈә
ёәј«___________________________Ј¬Хэј«______________________________ЎЈ
Ҫ«Ҫаҫ»өДҪрКфЖ¬AЎўBЎўCЎўD·Цұр·ЕЦГФЪҪюУРСОИЬТәөДВЛЦҪЙПГжІўС№ҪфЈЁИзУТНјЛщКҫЈ©ЎЈФЪГҝҙОКөСйКұЈ¬јЗВјөзС№ұнЦёХлөДТЖ¶Ҝ·ҪПтәНөзС№ұнөД¶БКэИзПВЈә

ҪрКф | өзЧУБч¶Ҝ·ҪПт | өзС№ЈЁVЈ© |
A | AЎъCu | + 0. 78 |
B | CuЎъB | 0.15 |
C | CЎъCu | + 1.35 |
D | DЎъCu | +0.30 |
ТСЦӘЈә№№іЙБҪөзј«өДҪрКфЖдҪрКф»оЖГРФПаІоФҪҙуЈ¬өзС№ұнөД¶БКэФҪҙуЎЈ
ЗлТАҫЭұнЦРКэҫЭЕР¶ПЈә
ЈЁ1Ј© ҪрКфҝЙДЬКЗЧоЗҝөД»№ФӯјБЈ» ҪрКфТ»¶ЁІ»ДЬҙУБтЛбНӯИЬТәЦРЦГ»»іцНӯЎЈ
ЈЁ2Ј©ИфВЛЦҪІ»УГСОИЬТәҪюИу¶шёДУГNaOHИЬТәҪюИуЈ¬ФтФЪВЛЦҪЙПДЬҝҙөҪөДА¶Й«іБөнОціцөДКЗ (МоЧЦДё)ҪрКфЎЈЖд¶ФУҰөДФӯөзіШөДөзј«·ҙУҰКҪОӘЈә
ёәј« Ј¬Хэј« ЎЈ
IЎўВБКЗөШҝЗЦРә¬БҝЧоёЯөДҪрКфФӘЛШЈ¬ЖдөҘЦКј°ЖдәПҪрФЪЙъІъЙъ»оЦРөДУҰУГК®·Ц№г·әЎЈ
(1)ҪрКфВБөДЙъІъКЗТФAl2O3ОӘФӯБПЈ¬Улұщҫ§КҜ(Na3AlF6)ФЪИЫИЪЧҙМ¬ПВҪшРРөзҪвЈ¬Фт»ҜС§·ҪіМКҪОӘЈә Ј®Ждөзј«ҫщУЙКҜД«ІДБПЧціЙЈ¬ФтөзҪвКұІ»¶ППыәДөДөзј«КЗ Ј»(МоЎ°Тхј«Ўұ»тЎ°Сфј«Ўұ)ЎЈ
(2)¶ФВБЦЖЖ·ҪшРРҝ№ёҜКҙҙҰАнЈ¬ҝЙСУіӨЖдК№УГКЩГьЈ®ТФҙҰАн№эөДВБІДОӘСфј«Ј¬ФЪH2SO4ИЬТәЦРөзҪвЈ¬ВБІДұнГжРОіЙСх»ҜДӨЈ¬Сфј«·ҙУҰКҪОӘ Ј»
(3)ВБөзіШРФДЬУЕФҪЈ¬Al-Ag2OөзіШҝЙУГЧчЛ®ПВ¶ҜБҰөзФҙЈ¬»ҜС§·ҙУҰОӘ2Al+3Ag2O+2NaOH+3H2OЁT2Na[Al(OH)4]+6AgЈ¬Фтёәј«өДөзј«·ҙУҰКҪОӘ Ј¬Хэј«ёҪҪьИЬТәөДpH (МоұдҙуЎўІ»ұд»тұдРЎ)ЎЈ
IIЎўөӘКЗөШЗтЙПә¬Бҝ·бё»өДТ»ЦЦФӘЛШЈ¬өӘј°Жд»ҜәПОпФЪ№ӨЕ©ТөЙъІъЎўЙъ»оЦРУРЧЕЦШТӘЧчУГЎЈ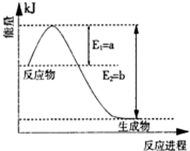
(1)НјКЗФЪТ»¶ЁОВ¶ИәНС№ЗҝПВN2әНH2·ҙУҰЙъіЙ1molNH3№эіМЦРДЬБҝұд»ҜКҫТвНјЈ¬ЗлРҙіцәПіЙ°ұөДИИ»ҜС§·ҙУҰ·ҪіМЈә (ЎчHөДКэЦөУГә¬ЧЦДёaЎўbөДҙъКэКҪұнКҫ)ЎЈ
(2)№ӨТөәПіЙ°ұ·ҙУҰИзПВЈ¬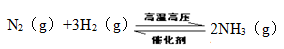
ФЪТ»¶ЁОВ¶ИПВЈ¬Ҫ«Т»¶ЁБҝөДN2әНH2НЁИлөҪМе»эОӘ1LөДГЬұХИЭЖчЦРЈ¬·ҙУҰҙпөҪЖҪәвәуЈ¬ёДұдПВБРМхјюЈ¬ДЬК№ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЗТЖҪәвіЈКэІ»ұдөДКЗ ЎЈ
| AЈ®ФцҙуС№Зҝ | BЈ®Фцҙу·ҙУҰОпөДЕЁ¶И | CЈ®К№УГҙЯ»ҜјБ | DЈ®ҪөөНОВ¶И |

°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com