
题目列表(包括答案和解析)
完成下列相关反应的化学方程式,离子反应只写离子方程式,氧化还原反应指出氧化剂、还原剂,并标出电子转移的方向和数目。
(1)Na与水反应生成NaOH和H2____________________________。
(2)一块除去氧化膜的铝片投放到Hg(NO3)2溶液中,一段时间后,取出铝片,露置于空气中,发现其表面长出大量的白毛,此现象称作“毛刷”现象______________________________________________。

某化学课外小组设计了如下图所示的装置,进行氨气性质实验。利用下图完成氨的催化氧化实验,其中箭头表示气体流向,A、B表示两种纯净、干燥的气体,反应进行一段时间后,装置已中有红棕色气体生成。实验中所用的药品和干燥剂只能从下列物质中选取KMnO4、Na2O2、NH4Cl、NH4HCO3、P2O5、碱石灰、生石灰、蒸馏水、浓硫酸、浓氨水
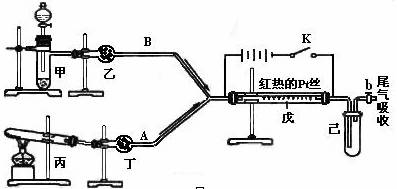
根据图I中装置和反应现象请回答:
(1)若乙中盛有P2O5,此时丙装置中发生反应的化学方程式为____________________。若丁中盛有P2O5,此时甲装置中应选择的试剂是____________________________。
(2)检验甲装置气密性的方法_________________________________________________
____________________________________________________________________________。
(3)当乙中充满红棕色气体后,停止甲、丙装置中的反应,并关闭a、b两个活塞,将己装置浸入冰水中,出现的现象是_______________________________________简述产生此现象的原因___________________________________________________________________
_______________________________________________________________________。
若将乙装置中的试管倒置于盛有水的水槽中,发生的现象是________________________。
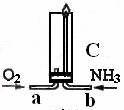
(4)已知氨气在纯氧中安静的燃烧,如下图,将过量O2与NH3分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气。先通入O2,后通过NH3的理由是
_____________________________________________________________________。
(5)液氨与水性质颇为相似,其电离方程式可表示为:2NH3![]() NH4++NH2-。某温度下其离子积常数为1×10-30(mol?L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
NH4++NH2-。某温度下其离子积常数为1×10-30(mol?L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
I.某校化学学习小组为了探究草酸(H2C2O4)的化学性质,设计了如下实验:
小组成员在做草酸溶液与酸性高锰酸钾溶液反应实验时发现,溶液褪色先慢后快。
(1)上述H2C2O4溶液与酸性KMnO4溶液反应的离子方程为 。
H2C2O4的电离方程式为
(2)为了探究此反应速率由小变大的原因,甲同学做了如下实验(表中“一”表示未加入该试剂)。
| 实验 编号 | 反应温度 (利用水浴加热) | 稀硫酸 溶液 | MnSO4固体 | 0.10 mol/L KMnO4溶液 | 褪色 时间 |
| 1 | 750C | 一 | 一 | 1mL | 100s |
| 2 | 750C | 10滴 | 一 | 1mL | 40s |
| 3 | 750C | 10滴 | 加入少许 | 1mL | 3s |
甲同学由此能够得出结论:
II.乙同学查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”, 决定用实验验证这一事实并检测草酸盐含量。进一步查阅资料得知,草酸(H2C2O4)是酸性强于醋酸的二元弱酸,对应的钙盐(CaC2O4)不溶于醋酸,能溶于强酸。
(1) 欲准确测定菠菜中草酸盐含量,回答有关问题:
①操作:取m g菠菜样品,将其中草酸盐转化为 CaC2O4 沉淀分离出来,用盐酸溶解后,溶液转入100mL容量瓶中加水配制成100mL溶液。每次移取25.00mL该溶液,用0.0100mol·L-1 KMnO4标准溶液滴定,滴定实验重复操作2 —3次。平均消耗标准溶液V mL。
②计算:菠菜中草酸盐(以C2O42-计)的质量分数为 。(只列式不计算,已知:C2O42-的的摩尔质量为88 g•mol-1)
③讨论:用标准KMnO4溶液直接滴定菠菜研磨、浸泡、过滤得到的溶液结果可能偏高,原因是 。
Ⅲ另一小组通过测定锌和不同浓度的稀硫酸反应来探究浓度对反应速率的影响(4mol/l稀硫酸,1 mol/l稀硫酸,Zn粒)。
所用装置如图:(1)如何检查该装置的气密性
(2)该实验除保证气密性良好外,还需注意: ,
(3)该小组同学所用实验时间相同,通过测定 来证明4mol/l稀硫酸反应速率快

Ⅳ.第四组完成温度对反应速度率的影响实验选择的药品为稀硫酸和硫代硫酸钠反应的方程式
为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com