
题目列表(包括答案和解析)
 (1)我国首创的海洋电池,总反应为:4Al+3O2+6H2O=4Al(OH)3,负极为:
(1)我国首创的海洋电池,总反应为:4Al+3O2+6H2O=4Al(OH)3,负极为: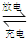 2PbSO4+2H2O放电时,正极电极反应式
2PbSO4+2H2O放电时,正极电极反应式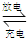
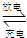 2PbSO4+2H2O放电时,正极电极反应式______,当电路中通过0.5mol电子时,消耗H2SO4的物质的量______,负极增重______g.
2PbSO4+2H2O放电时,正极电极反应式______,当电路中通过0.5mol电子时,消耗H2SO4的物质的量______,负极增重______g.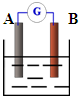
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com