
题目列表(包括答案和解析)
| |||||||||||||||||||||||
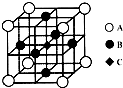 (2013?南通一模)【物质结构与性质】
(2013?南通一模)【物质结构与性质】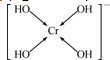

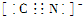
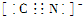
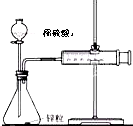 通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:
通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:| 序号 | Na2S2O3溶液 | 稀H2SO4 | 出现混浊时间 | ||
| 浓度 | 用量 | 浓度 | 用量 | ||
| (1) | 0.1mol?L-1 | 10mL | 0.1mol?L-1 | 10mL | t1 |
| (2) | 0.1mol?L-1 | 10mL+5mL 水 | 0.1mol?L-1 | 10mL | t2 |
| (3) | 0.1mol?L-1 | 10mL | 0.1mol?L-1 | 5mL+5mL水 | t3 |
| (4) | 0.1mol?L-1 | 5mL | 0.1mol?L-1 | 5mL | t4 |
K2Cr2O7是一种橙红色具有强氧化性的化合物,当它在酸性条件下被还原成三价铬时,颜色变为绿色.据此,当交警发现汽车行驶不正常时,就可上前阻拦,并让司机对填充了吸附有K2Cr2O7的硅胶颗粒的装置吹气.若发现硅胶变色达到一定程度,即可证明司机是酒后驾车.这时酒精(CH3CH2OH)被K2Cr2O7氧化为醋酸(CH3COOH)。该氧化还原反应的方程式可表示为:
2K2Cr2O7+3CH3CH2OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O
思考:被检测的气体成分是________________,上述反应中氧化剂是________________,还原剂是_______________________。
怎样判断司机是否酒后驾车
K2Cr2O7是一种橙红色、具有强氧化性的化合物,当它在酸性条件下被还原成三价铬时,颜色变为绿色。据此,当交警发现汽车行驶不正常时,就可上前阻拦,并让司机对填充了吸附有K2Cr2O7的硅胶颗粒的装置吹气。若发现硅胶变色达到一定程度,即可证明司机是酒后驾车。这时酒精(CH3CH2OH)被K2Cr2O7氧化为醋酸(CH3COOH)。
该氧化还原反应的方程式可表示为:
2K2Cr2O7+3CH3CH2OH+8H2SO4→2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O
思考:在这一反应中,氧化剂是_______________,还原剂是______________,氧化产物是________________,还原产物是_______________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com