A.大量的
SO2
SO2
和
氮的氧化物
氮的氧化物
扩散到大气中,在空气.阳光等作用下发生一系列变化,遇雨时被雨水吸收,当雨水的pH小于
5.6
5.6
时就形成了酸雨.
某校科技小组的同学们采集酸雨样品,每隔一段时间测定样品的pH,得到下列数据:
| 时间 |
开始 |
8h后 |
16h后 |
24h后 |
32h后 |
40h后 |
48h后 |
| pH |
5.0 |
4.8 |
4.5 |
4.3 |
4.2 |
4.0 |
4.0 |
回答下列问题:
(1)酸雨放置时,pH发生变好的主要原因为
雨水中亚硫酸被氧化成硫酸,酸性增强
雨水中亚硫酸被氧化成硫酸,酸性增强
.
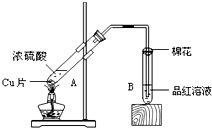
(2)煤中含有游离态的硫,试写出它经过一系列变化最后变成酸雨主要成分的有关化学方程式.(空线不一定填满)
,
2SO2+O2=2SO3
2SO2+O2=2SO3
,
SO3+H2O═H2SO4
SO3+H2O═H2SO4
,
无
无
.
B.有A.B两种烃,它们的组成相同,都约含85.7%的碳,烃A对氢气的相对密度是28;烃B式量比空气的平均式量稍小,且最简式与A相同,烃A.B都能使溴的四氯化碳溶液褪色,根据以上实验事实计算并回答问题.
(1)推算A.B两烃的化学式.(推算步骤写在下面)
A
C4H8
C4H8
;B
C2H4
C2H4
.
(2)A、B中
C4H8
C4H8
(填A.B的分子式)存在同分异构体.
(3)写出B与溴的四氯化碳溶液反应的化学方程式:
CH2=CH2+Br2→CH2Br-CH2Br
CH2=CH2+Br2→CH2Br-CH2Br
.