
题目列表(包括答案和解析)
某化学课外活动小组用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉,现已知反应2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,正反应为放热反应,温度稍高即发生副反应6Cl2+
6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。甲、乙、丙三人分别设计三个实验装置,如下图所示。
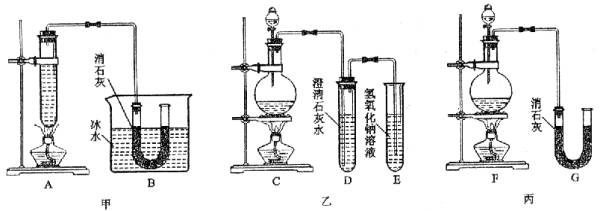
(1)请指出三个装置各处的缺点或错误(如没有可不填)
甲:_______________________________________________________;
乙:_______________________________________________________;
丙:_______________________________________________________。
(2)图甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G组成,从上述甲、乙、丙三套装置中选出合理的部分(按气流从左到右的方向)组装一套较完善的实验装置(填所选部分的编号) ___________________________________。
(3)实验中若用12mol·L-1的浓盐酸100mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是小于0.15mol,其可能的主要原因是(假定各步反应均无反应物损耗且无副反应发生) _______________________________________________________。
(10分)某化学兴趣小组利用浓盐酸、二氧化锰共热制氯气,并用氯气和消石灰制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2 = Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应。试回答以下问题: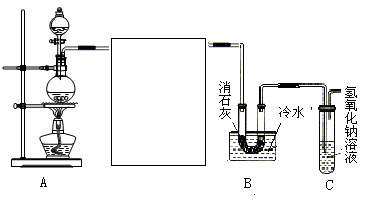
(1)制取氯气时在烧瓶中加入一定量的二氧化锰,通过 (填仪器名称)向烧瓶中加入适量的浓盐酸,写出该反应的离子方程式 。
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内(示意图),并注明其中盛放的药品。如果A产生的气体直接进入B中,实验产生的不良后果是 。
(3)实验室若用16 mol ?L-1的盐酸100 mL与足量的二氧化锰反应,理论上最终生成的Ca(ClO)2的物质的量最多不超过 mol。
(10分)某化学兴趣小组利用浓盐酸、二氧化锰共热制氯气,并用氯气和消石灰制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2 Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应。试回答以下问题: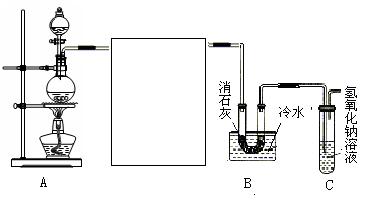
(1)制取氯气时在烧瓶中加入一定量的二氧化锰,通过 (填仪器名称)向烧瓶中加入适量的浓盐酸,写出该反应的离子方程式 。
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内,并注明其中盛放的药品。如果A产生的气体直接进入B中,实验产生的不良后果是 。
(3)实验室若用16 mol·L-1的盐酸100 mL与足量的二氧化锰反应,理论上最终生成的Ca(ClO)2的物质的量最多不超过 mol。
现用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉.现已知反应2Cl2+2Ca(OH)2 Ca(ClO)2+CaCl2+2H2O,温度稍高即发生副反应
Ca(ClO)2+CaCl2+2H2O,温度稍高即发生副反应
 5CaCl2+Ca(ClO3)2+6H2O.甲、乙、丙三人分别设计三个实验装置,如下图示:
5CaCl2+Ca(ClO3)2+6H2O.甲、乙、丙三人分别设计三个实验装置,如下图示:
(1)请从以下几个方面对上述甲、乙、丙三套装置的优缺点作出评析,并选择符合题目要求的选项填在表格内:
a.不容易控制反应速率
b.容易控制反应速率
c.有副反应发生
d.可防止副反应发生
e.污染环境
f.可防止污染环境
(2)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成,从上述甲、乙、丙三套装置中选出合理的部分(按气流从左到右的方向),组装一套较完善的实验装置(填编号)________.
(3)实验中若用12 mol/L的浓盐酸100 mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总小于0.15 mol(假定各步反应均无反应损耗且无副反应发生),其可能的主要原因是________.
实验室用浓盐酸、MnO2共热制Cl2,再用Cl2和Ca(OH)2反应制少量漂白粉。现已知反应:
2Cl2+2Ca(OH)2![]() Ca(ClO)2+CaCl2+2H2O
Ca(ClO)2+CaCl2+2H2O
温度稍高即发生副反应:6Cl2+6Ca(OH)2![]() Ca(ClO3)2+5CaCl2+6H2O
Ca(ClO3)2+5CaCl2+6H2O
现有三个同学分别设计的三套实验装置如下:
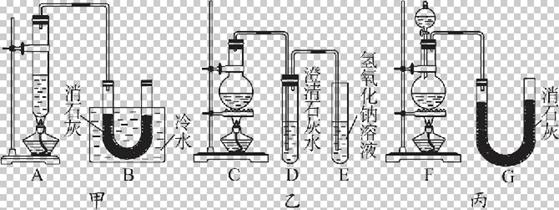
(1)请从①不容易控制反应速率,②容易控制反应速率,③有副反应发生,④可防止副反应发生,⑤污染环境,⑥可防止污染环境几个方面对上述甲、乙、丙三套装置的优缺点作出评析,并选择符合题目要求的选项填在空格内。
| 优点 | 缺点 | |
| 甲装置 | ||
| 乙装置 | ||
| 丙装置 |
(2)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,再由F、G两部分组成。请从上述装置中,选取合理的组成部分,组装一套较完善的实验装置,装置各部分的连接顺序(按气流从左到右的方向)是________________________。
(3)实验中若用12 mol·L-1的浓盐酸100 mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量_______________0.15 mol(填“大于”“小于”或“等于”),其原因是____________(假定各步反应均无反应物损耗,且无副反应发生)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com