
题目列表(包括答案和解析)
加热N2O5时,发生以下两个分解反应:
N2O5![]() N2O3+O2
N2O3+O2
N2O3![]() N2O+O2
N2O+O2
在1L密闭容器中加热4mol N2O5达到化学平衡时,c(O2)为4.5mol·L-1,c(N2O3)为1.62mol·L-1,则在该温度下各物质的平衡浓度不正确的是
[ ]
A.c(N2O5)平=1.44mol·L-1
B.c(N2O5)平=0.94mol·L-1
C.c(N2O)平=1.44mol·L-1
D.c(N2O5)平=3.48mol·L-1
加热N2O5时发生以下两个分解反应:N2O5(g)![]() N2O3(g)+O2(g),N2O3(g)
N2O3(g)+O2(g),N2O3(g)![]() N2O(g)+O2(g),在1L密闭容器加热4mol N2O5,达到平衡时O2的浓度为4.5mol·L-1,N2O3的浓度为1.62mol·L-1.则在该温度下,各物质平衡浓度正确的是
N2O(g)+O2(g),在1L密闭容器加热4mol N2O5,达到平衡时O2的浓度为4.5mol·L-1,N2O3的浓度为1.62mol·L-1.则在该温度下,各物质平衡浓度正确的是
[ ]
A.N2O5的浓度为1.44mol·L-1
B.N2O5的浓度为0.94mol·L-1
C.N2O的浓度为1.44mol·L-1
D.N2O的浓度为3.48mol·L-1
某硝酸厂附近的空气主要污染物为氮的氧化物.为了保护环境和综合利用,可采用氨-碱两级吸收法.此法兼有碱吸收和氨吸收两法的优点,其吸收工艺流程如下:
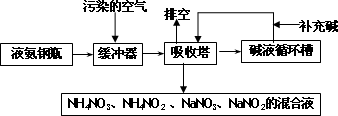
(1)排空物质的主要成分为________.
(2)进入吸收塔以前加一个缓冲器的目的是________.
(3)从吸收塔排出的混合液用途之一为________.
空气的主要污染物为硫的氧化物和氮的氧化物.研究人员设计了同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如下:
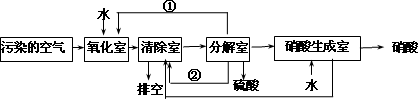
各室中发生的反应如下:
a.氧化室:NO2(g)+SO2(g)+H2O(l)![]() H2SO4(l)+NO(g) ΔH=akJ·mol-1
H2SO4(l)+NO(g) ΔH=akJ·mol-1
b.清除室:NO(g)+NO2(g)=N2O3(g) ΔH=b kJ·mol-1
N2O3(g)+2H2SO4(l)![]() 2NOHSO4(s)+H2O(l) ΔH=c kJ·mol-1
2NOHSO4(s)+H2O(l) ΔH=c kJ·mol-1
c.分解室:4NOHSO4(s)+O2(g)+2H2O(l)![]() 4H2SO4(l)+4NO2(g) ΔH=d kJ·mol-1
4H2SO4(l)+4NO2(g) ΔH=d kJ·mol-1
回答下列问题:
(4)①和②分别为(写化学式)________、________.
(5)写出SO2、O2和H2O反应生成H2SO4的热化学方程式:________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com